- cis-ジオール,trans-ジオールの合成法が説明できる
- 四酸化オスミウムがなぜ触媒利用されるか説明できる
- 過ヨウ素酸ナトリウムがなぜvic-ジオール選択的に酸化開裂するか説明できる
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に
「理解でつなぐ大学有機化学」をかわいくお届けします。

アルケンを二つのカルボニル基に“酸化開裂する”変換。
多くの人が最初に思い浮かべるのは、前回あつかったオゾン分解かもしれません。
でも、一つの化学変換に対する引き出しが一つだと困る場面があります。
実験では、同じ変換でも反応条件の相性の良し悪しが基質ごとに変わるからです。
(良い収率になるまで総当たりになることも、、、)
大事なのは、反応名を一つ覚えることよりも、その変換に到達する“別ルート”を複数持っておくこと。
そして、どのルートが今の目的に合うかを比べられること。
ということで今回は、オゾン分解“以外”でアルケンを酸化開裂へ導く経路を整理していこうと思います。
ルートを並べて、基質の形(鎖状/環状)、試薬の扱いやすさ、経由する官能基といった違いに着目しつつ反応機構を学習していきます。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
文字が苦手な人も図を追えるように構成しているので、参考書のつもりでゆっくりどうぞ。
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
全体像:アルケン酸化開裂の主要3経路と押さえるポイント
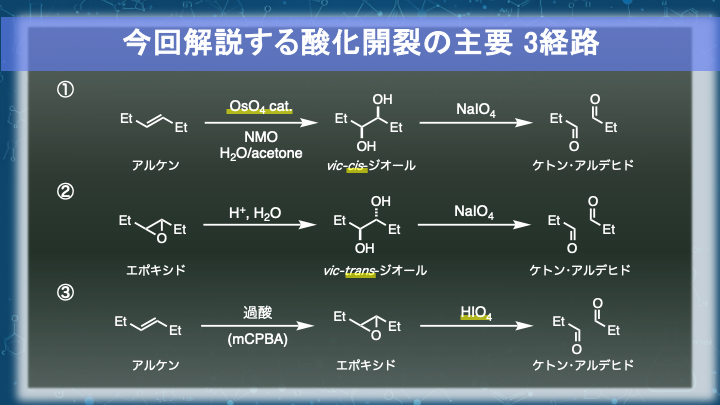
アルケンを二つのカルボニル基に酸化開裂する方法は、オゾン分解以外にもいくつか存在します。
この講義では、代表的な経路を3つ取り上げます。
-
経路①
アルケンを四酸化オスミウムで vic-cis-ジオール に変換し、それを過ヨウ素酸ナトリウムで酸化開裂する方法 -
経路②
アルケンをエポキシ化し、酸性条件で開環して vic-trans-ジオール を経由する方法
(主に鎖状アルケンで使われます) -
経路③
vic-ジオールではなくエポキシを経由し、過ヨウ素酸で直接酸化開裂させる方法
(発展的な内容です)
最終的な官能基変換は同じでも、途中で通る構造や条件は大きく異なります。

ここで、この講義で必ず持ち帰ってほしいポイントを先にまとめておきます。
理由や詳しい説明は、後の章で順に確認していきます。
- 四酸化オスミウムはアルケンにシン付加し、 vic-cis-ジオール を与える
- 四酸化オスミウムは毒性が高いため、 触媒量使用+再酸化剤の併用が標準である
- エポキシの開環は背面攻撃で進行し、 vic-trans-ジオール を与える
- 過ヨウ素酸はヨウ素のオキソ酸の中で 最も酸化度が高い
- vic-ジオールの酸化開裂は 五員環中間体の形成を経由して進行する
読み終えたあと、もう一度このリストに戻ってみてください。
授業を思い返しながら、リストを確認すると効率10倍です!
前回取り扱ったオゾン分解と比較しながら読めるようになると、
一段レベルアップです。
四酸化オスミウムによるcisジオール化
反応機構の全体の流れを確認

反応の全体像を先に押さえておくと、
このあと登場する反応機構の意味が、流れとして理解できるようになります。
四酸化オスミウムによるアルケンのcisジオール化は、次の三つの段階から成り立っています。
- 1. アルケンと四酸化オスミウムが協奏的に反応し、五員環オスメートを形成する段階
- 2. そのオスメートが加水分解され、アルケン由来のジオールが遊離する段階
- 3. 反応の過程で還元されたオスミウムが、再酸化剤によって元の状態に戻される段階
この反応で導入される官能基は、隣接する二つの炭素に同じ向きで水酸基が導入された vic-cis-ジオールです。
ここで酸化数に注目すると、オスミウムは +8 から +6 へと還元され、
一方でアルケン側の二つの炭素はC–O結合の形成によって形式的に +2 酸化されています。
電子は酸化を受ける分子から酸化剤へと流れます。
電子をどこに受け取っているのか、丁寧に追うことで反応機構をミスなく記述できます。
反応機構解説① 双極付加環化
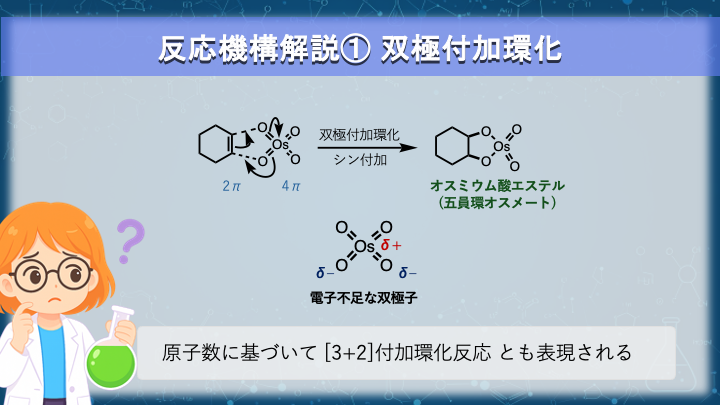
四酸化オスミウム(OsO₄)は、オスミウム原子を中心に
Os=O 結合を4本 持つ構造をしています。
重原子であるオスミウムは多数の結合を取ることができ、それぞれの酸素原子は強く電子を引きつけています。
そのため、オスミウム中心は全体として電子不足な状態にあり、
Os=O を含む三原子ユニット(O–Os–O)は電子の偏りをもった反応単位として振る舞います。
この三原子ユニットがアルケンの二原子ユニットと反応することで、
五員環を形成する 1,3-双極付加環化反応 が進行します。
付加環化の基本に立ち返ると、四酸化オスミウム側の反応点には
二つの Os=O に由来する 4π 電子が関与し、アルケンの 2π 電子と組み合わさって
付加環化が進行していると整理できます。
双極子とアルケンの原子数に基づいて、[3+2]付加環化反応 と表現することもあります。
「双極付加って何だったっけ?」となったら、
オゾン分解の記事で一度整理してから戻ってきてもOKです。
このとき、OsO₄ の酸素由来の電子とアルケンの π 電子が同時に再配置され、新たに 2 本の C–O σ結合が一度に形成されます。
こうして生成する五員環中間体をオスミウム酸エステル(五員環オスメート)と呼びます。
五員環を形成するという空間的制約のため、二つの C–O 結合は必ず同じ側から導入されます。
その結果、この反応では シン付加が起こり、アルケンからは vic-cis-ジオールが得られます。
(vic はビシナルと発音します)
vic は vicinal(ラテン語で「隣り合った」)に由来する接頭辞です。
vic-ジオールは「隣接した2つの炭素に水酸基がある」構造を指します。
反応機構解説② オスメートの加水分解
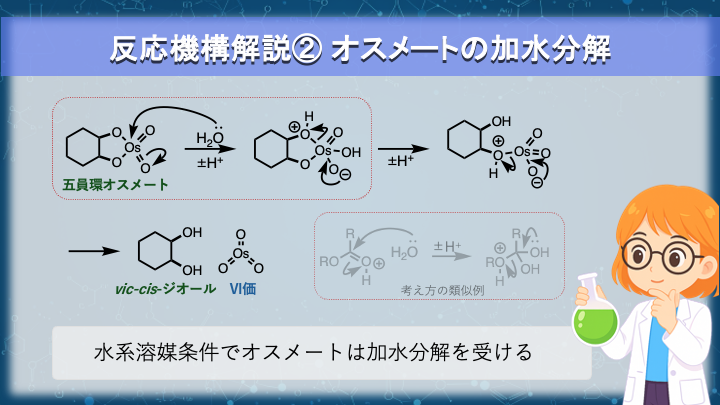
四酸化オスミウムによるcisジオール化は、BuOH/H2O や acetone/H2O など、水を含む溶媒系で行われます。
この反応条件では、五員環オスメートは単離されることなく、加水分解反応が進行します。
水分子がオスミウム原子に求核攻撃すると、五員環構造が開裂し、オスミウム–酸素結合が切断されます。
続くプロトン移動によって、アルケン由来の炭素上に水酸基が生成します。
この加水分解が両側で起こることで、vic-ジオールが得られ、オスミウムは還元状態(Ⅵ)として反応系に残ります。
この一連の電子の流れを理解する私なりのコツとしては、カルボン酸誘導体の加水分解とよく似た形式を持っていると考えることです。(赤囲いを比較)
水分子が電子不足なオスミウム原子に求核付加し、一度、四面体型の中間体を経由した後、酸素原子側が脱離基を押し出す形で分解が進みます。
その結果、アルコールと還元状態のオスミウム酸(Ⅵ)が生成します。
反応機構は「まったく新しいもの」として覚えるよりも、
知っている反応と共通項で整理すると、
理解が一気に楽になりますね。
OsO4は危険で高価:触媒化が標準になる理由
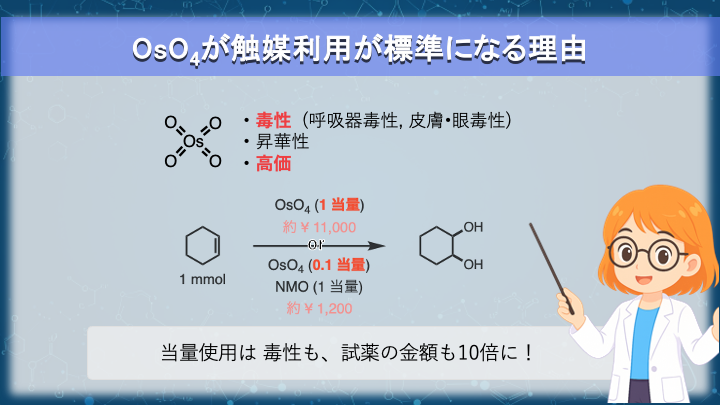
四酸化オスミウムは、反応性の高い優れた酸化剤である一方、実験条件の設計には注意が必要な試薬です。
まず、安全面の観点から見ると、四酸化オスミウムは強い毒性を示します。
特に、蒸気の吸入による急性毒性や、皮膚・眼への重篤な障害が報告されており、毒性区分としては最も危険な区分1に分類されています。
特に、蒸気の吸入による急性毒性や、皮膚・眼への重篤な障害が報告されており、毒性区分としては 最も危険な区分1 に分類されています。
さらに、昇華しやすい性質を持つため、濃縮操作では換気ドラフト内での取り扱いが求められます。
次に、コストの問題があります。
例えば東京化成(TCI)では、4%四酸化オスミウム水溶液 10 mL が約 17,900 円(2025年12月現在)で販売されています。
仮に 1 mmol のアルケンを当量の四酸化オスミウムでジオールへ変換しようとすると、
約一万円規模 の試薬を消費する計算になります。
これらを踏まえると、アルケンのシスジオール化を行う際に四酸化オスミウムを当量用いる方法は、安全面・経済面の両方から見て 合理的とは言えません。
そのため実際の反応設計では、ジオール化の過程で還元された Ⅵ価のオスミウムを再酸化し、触媒量で反応を進行させる手法が標準的に用いられます。
再酸化機構解説
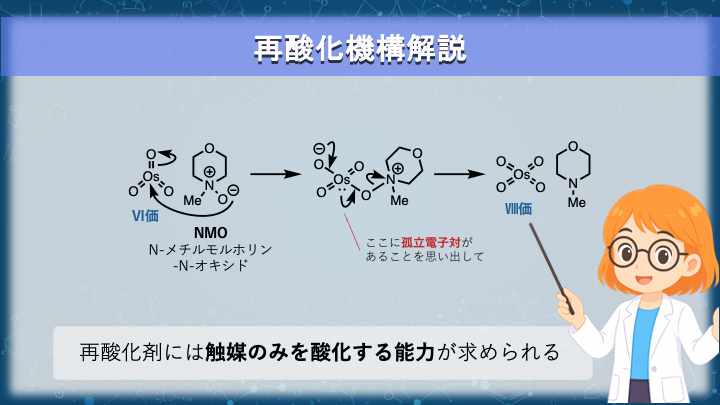
触媒量の四酸化オスミウムによるシスジオール化では、ジオール生成の過程でオスミウムは Ⅷ価 から Ⅵ価 へと還元されます。
このままでは反応はワンサイクルで止まってしまいます。
そこで必要になるのが、還元されたオスミウムを再びⅧ価へ戻す「再酸化」の操作です。
再酸化剤は、触媒と共存させてオスミウムに渡った電子を受け取り、触媒サイクルを閉じる役割を果たします。
実際に用いられる再酸化剤には、次のようなものがあります。
① N-メチルモルホリンオキシド(NMO)
② フェリシアン化カリウム K₃[Fe(CN)₆]
③ 過酸化水素 H₂O₂
④ tert-ブチルヒドロペルオキシド t-BuOOH
⑤ 過ヨウ素酸ナトリウム NaIO₄
(ジオールの酸化開裂も連続して起こる)
まずは、電子の流れが最も追いやすいNMOを例にして見てみましょう。
Ⅵ価の酸化オスミウムに対して、NMOの酸素原子の孤立電子対が配位し、一時的な錯体を形成します。
その後、N-メチルモルホリンが脱離し、電子不足となった酸素へオスミウムから電子対が戻されます。
ジオール化の第一段階で酸素からオスミウムへ電子対が移動したことを思い出してください。
再酸化では、その電子の流れを逆向きに戻していると考えると理解しやすいでしょう。
重原子の電子状態わからなくて怖くなりがち。
今回は付加環化の時の動きの逆回りだから、安心できるね!
経路②:エポキシ開環でvic-trans-ジオールを作る
ジオールは四酸化オスミウム以外を用いても得ることができます。
反対の相対配置である transジオール を得ることができる手法として、
エポキシを経由する手法を紹介します。
アルケンをエポキシドに変換する反応については、#U3ですでに解説しています。
内容に自信のない人や、まだ見たことのない人は復習をしてから次に進んでくれると嬉しいです。
反応機構解説:歪みと酸の活性化による分極が開環を駆動する
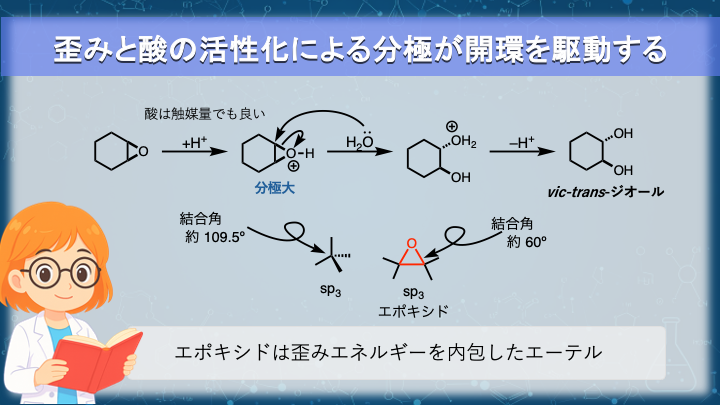
この反応で最も重要だと言いたいことは、
「エポキシドは特殊な官能基」ではなく、エーテルの一種である
と理解することです。
通常の鎖状エーテルでは、C–O 結合は比較的安定で、穏やかな条件下で置換反応が進行することはほとんどありません。
ところがエポキシドでは、同じ C–O 結合を持ちながら、弱い条件でも開環反応が進行します。
この違いを生んでいるのが、三員環構造に由来する大きな歪みです。
sp³ 混成原子が本来とりたい結合角は約 109.5°ですが、
三員環ではそれが強制的に約 60°まで押し込められています。
エポキシドは、結合を保っているだけでエネルギーを蓄え続けているエーテルだと考えることができます。
このような窮屈な結合角によって蓄えられるエネルギーを歪みエネルギーと言います
さらに、酸性条件下ではエポキシドの酸素原子がプロトン化され、C–O 結合の分極が強まり、炭素原子の求電子性が一段高まります。
その結果、鎖状エーテルでは反応に参加できないような弱い求核剤であっても、「歪みを解消する」という駆動力に後押しされてC–O 結合の切断が進行します。
置換反応についてはブルースの9〜11章の内容を取り扱うときに丁寧に説明し直します。
背面攻撃がtrans配置を与える
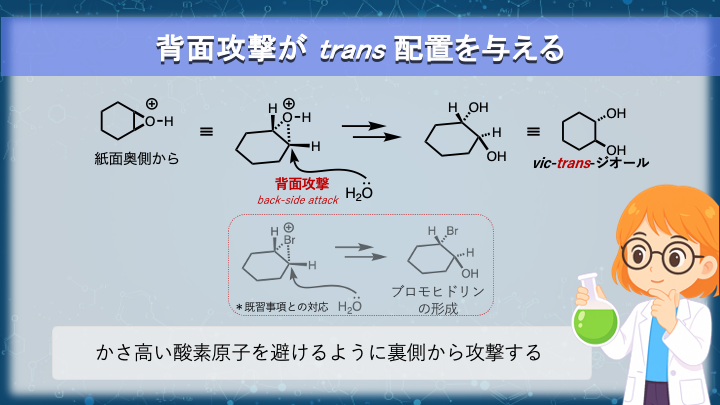
環状ジオールには、環の同じ側に官能基のある cis(syn) 体と、反対側に官能基のある trans(anti) 体が存在します。
四酸化オスミウムで作るジオールはcisであることを解説しました。
今回のエポキシの開環で得られるジオールはどうでしょう。
結論としては、環の反対側同士にヒドロキシ基が導入されたtrans ジオールが生成します。
エポキシの開環は水分子の背面攻撃により進行するため、二つの C–O 結合はtransで形成されます。
エポキシの切れる結合と、新しく作られるC–O結合は一直線上に並びます。
求核剤が到達したい核(炭素原子)へは、三員環の裏側からのアプローチが最も合理的で反発が少ないのです。
#U3 ではハロゲンの付加反応について解説していますが、
この反応で起こる環状ブロモニウムイオンへの求核攻撃と全く同じ理由です。
過ヨウ素酸ナトリウム(NaIO4)を“書ける”ようにしてから機構へ進む
ここまでで、隣接したジオール(vic-ジオール)をどのように作るかを見てきました。
次に登場するのが、この vic-ジオールを二つのカルボニル基へと酸化開裂させる 過ヨウ素酸ナトリウム(NaIO₄) です。
この反応の反応機構を書けと問われると多くの人が同じところで手が止まるのではないでしょうか。
「NaIO₄ の構造が書けない」
まずはこの不安を解消してから、反応機構へ進むことにしましょう。
HIO4はヨウ素のオキソ酸:型で捉える
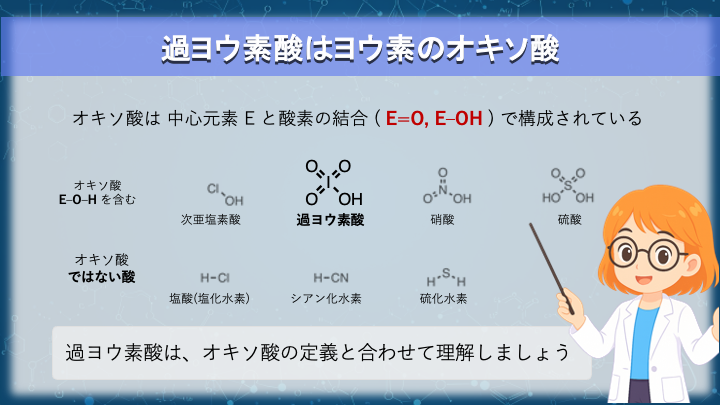
過ヨウ素酸は HIO₄ という分子式をもつヨウ素のオキソ酸の一種です。NaIO₄ は、そのナトリウム塩にあたります。
オキソ酸とは、中心元素と酸素を介してプロトンが結合した酸のことです。
構造としては必ず、
- 中心元素 E (ヨウ素)
- E=O
- E–OH
という組み合わせを含みます。
例えば、HCl のようなハロゲン化水素やHCN などの有機酸は、酸ではありますが、酸素を介したプロトンではないためオキソ酸ではありません。
一方で、硫酸(H₂SO₄)や硝酸(HNO₃)は、この「中心元素+酸素」という型を満たしています。
過ヨウ素酸がどんな酸の分類なのか理解することがより効率的でケアレスミスの少ない暗記手法になるのです。
接頭辞は酸化数の情報:過/亜/次亜の意味
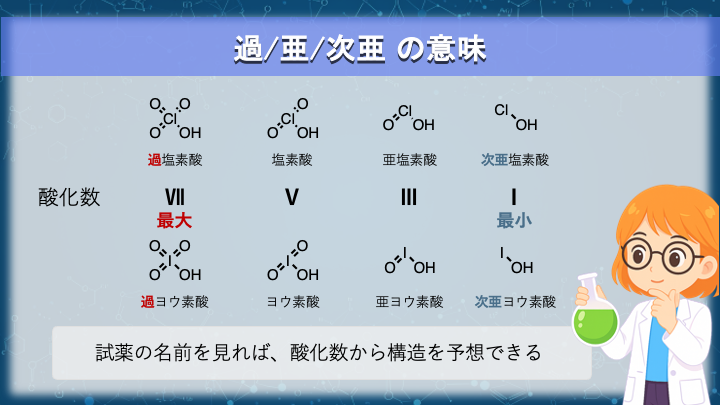
ヨウ素のオキソ酸は、実は複数種類考えることができます。
このとき手がかりになるのが、名前の前につく接頭辞です。
「過」 は、中心元素が取りうる 最大の酸化数 を意味します。
過ヨウ素酸(HIO₄)では、ヨウ素の 価電子(7つ) がすべて
素との結合に使われています。
反対に、「次亜」 は最小の酸化数を表します。ハロゲンでは X–OH の形がこれに対応し、
次亜塩素酸が代表例です。
その中間にあたるものが「亜」、そして接頭辞のつかないヨウ素酸(HIO₃)が基準になります。
つまり、名前を見れば、酸化数がわかるというわけです。
ここまでくれば、HIO₄ という分子式も、NaIO₄ の構造も、「暗記」ではなく
数学の定理のように”導出できる“ようになります。
暗記の早さと深さは違うと感じています。
深い暗記を目指して少し遠回りするのも、
付随する知識が増えてお得かも?
ジオールのマラプラードグリコール開裂反応機構
反応機構の全体の流れを確認

ここからが本題です。
vic-ジオールを過ヨウ素酸(NaIO₄ / HIO₄)で酸化開裂し、二つのカルボニル化合物に変える反応を マラプラード(Malaprade)グリコール開裂と呼びます。
反応の全体像を先に押さえておくと、このあと登場する反応機構の意味が、流れとして理解できるようになります。
この反応でまず押さえるべきポイントは、
“五員環の中間体(周期酸エステル)”を経由することです。
この中間体ができるからこそ、その後の開裂が起こります。
だからこそ、五員環中間体を形成するvic-ジオールを選択的に酸化開裂させることができるのです。
全体の流れは次の3ステップです。
- 1. vic-ジオールの2つの酸素が、ヨウ素中心に結合して 五員環の周期酸エステル(中間体)をつくる
- 2. 中間体が崩れてC–C結合が開裂し、同時にヨウ素は Ⅶ価 → Ⅴ価へ還元される
- 3. 2つのカルボニル化合物が生成する(アルデヒド/ケトン)
この酸化開裂反応は官能基選択性がよく、
vic-ジオールやその他一部の酸化されやすい原子(S,P) のみが反応します。
反応機構解説① ジオールの付加
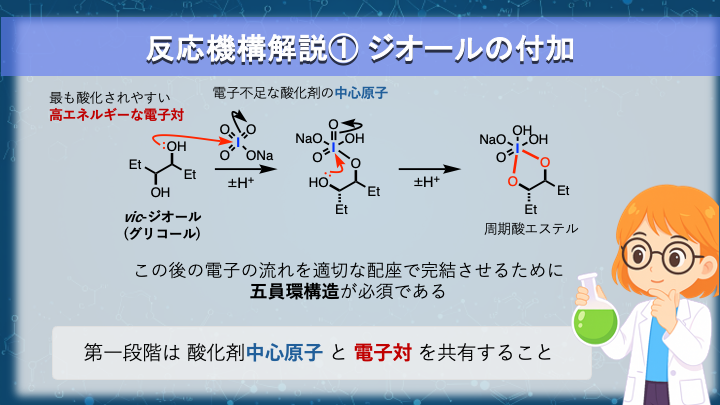
過ヨウ素酸による酸化開裂反応を理解するうえで、最初に押さえておきたいことを述べます。
電子の授受が起こるためにはまず、電子を受け取りたい原子と電子を渡すことができる電子対が、同じ構造の中で直接結びつく必要があるということです。
今回、酸化数が変化するのはヨウ素原子です。
過ヨウ素酸中のヨウ素は高い酸化状態(Ⅶ価)にあり、周囲を複数の酸素原子に囲まれた、電子不足な中心原子として振る舞います。
一方、基質である vic-ジオールには、二つの酸素原子が隣接して存在し、それぞれが高エネルギーな孤立電子対を持っています。
この二つの電子対こそが、この反応で最も反応性の高い「電子の供給源」です。
まず起こるのは、vic-ジオールの二つの酸素原子がヨウ素中心に向かって結合を形成する過程です。
このとき、過ヨウ素酸の I=O 結合が切れ、ヨウ素と二つの酸素が結びついた五員環の周期酸エステル中間体が生成します。
重要なのは、二つの水酸基のうち一方のみが結合を形成するわけではなく、両方がヨウ素と結合を作って五員環をつくるという点です。
この五員環中間体が形成されたことで、初めて次の電子の流れが内部で完結できる状態が整い、
C–C 結合の開裂が進行します。
酸化反応は電子がヘテロ原子から、酸化剤中心に流れます。
電子が流れるためには、まずは動く電子が共有結合で結ばれる必要があるのです。
反応機構解説② 五員環中間体から酸化開裂
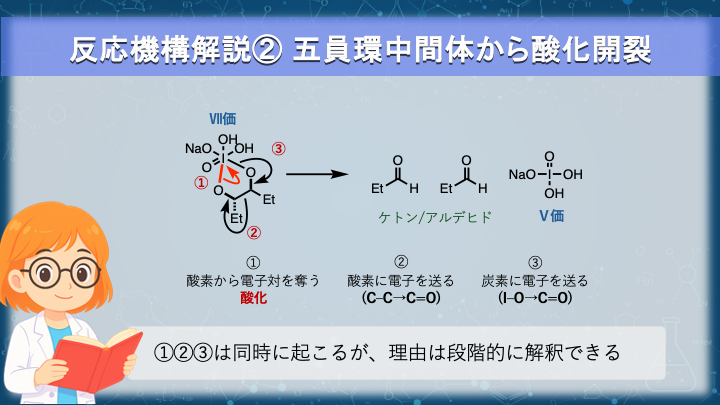
五員環の周期酸エステル中間体が形成されると、分子内で電子のやり取りが完結できる状態になります。
ここから起こるのが、いわゆる「酸化開裂」です。
過ヨウ素酸中のヨウ素原子は、高い酸化状態(Ⅶ価)にあるため、分子内で電子を受け取れる機会を常に探しています。
五員環中では、
① ヨウ素は隣接する I–O 結合から電子を引き寄せ、より安定な低酸化状態(Ⅴ価)へ移行しようとします。
しかし、I–O 結合の電子がヨウ素側へ引き抜かれると、対応する酸素原子は電子不足な状態になります。
② この電子不足を埋めるために、隣接する C–C 結合が電子を供給するしかなくなります。
その結果、C–C 結合は開裂し、
③ 電子が移動した炭素には、I–O結合電子が流れ、カルボニル基を形成します。
この反応では、分子内の電子の需給バランスが、C–C 結合に切断という役割を押し付けていると理解すると、流れを理解しやすくなります。
複数の電子の流れは、起点となる反応の駆動力の本質から丁寧に理解していきましょう
五員環を作れる vic-cis (syn)-ジオールのみ反応する
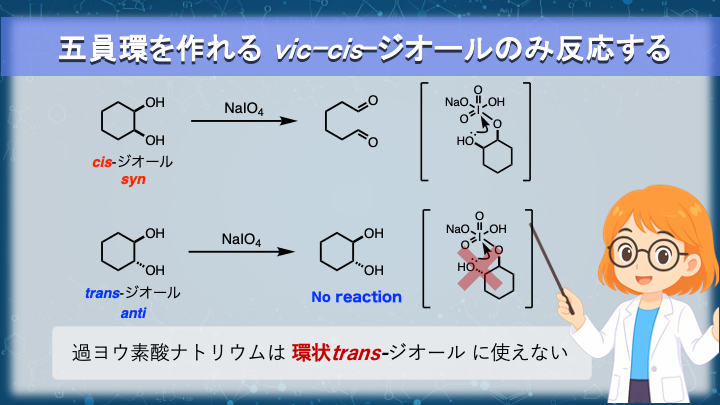
過ヨウ素酸による酸化開裂は、すべての vic-ジオールに等しく適用できる反応ではありません。
特に環状基質では、ジオールの立体配置が反応そのものを左右します。
この反応は、vic-ジオールが過ヨウ素酸と結合して五員環中間体を形成できることを前提としています。
したがって、五員環を作れない配置では反応は進行しません。
シクロヘキサン-1,2-ジオールを例に考えると、
cis体では五員環中間体が形成可能で、酸化開裂が起こります。
一方、trans体ではこの中間体を構築できず、反応は起こりません。
この違いは、ジオールの作り方に直結します。
鎖状アルケンから出発する場合は、四酸化オスミウムによるcisジオール化でも、エポキシ開環によるtransジオール化でも、どちらを経由しても酸化開裂が可能です。
しかし環状アルケンを出発原料とする場合、エポキシ経由でtransジオールを作ってしまうと、過ヨウ素酸による開裂に進めません。
この場合は、四酸化オスミウムを用いてcisジオールを与えるルートを選ぶ必要があります。
反応機構の理解は、最終的に「どのルートを選ぶか」というルート戦略に結びつきます。
OsO4/NaIO4でワンポット酸化開裂
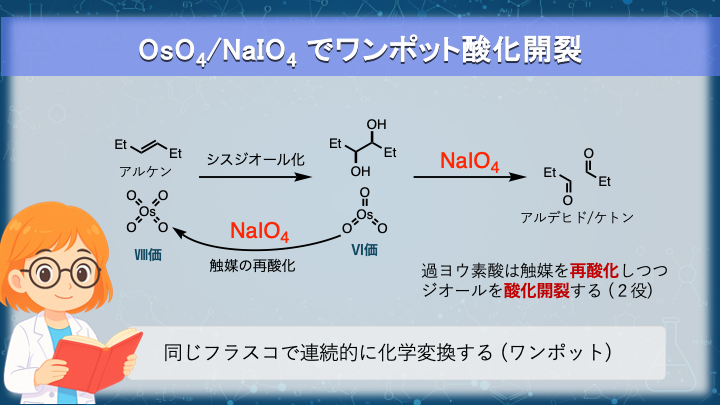
過ヨウ素酸ナトリウムは、vic-ジオールを酸化開裂させる試薬であると同時に、四酸化オスミウムを再酸化する再酸化剤としても働きます。
この二つの役割が、同じ反応系の中で両立できる点が重要です。
まず、触媒量の四酸化オスミウムによってアルケンはcisジオールへと変換されます。
この過程で還元されたオスミウムは、過ヨウ素酸ナトリウムにより再酸化を受け触媒サイクルが維持されます。
一方で、生成した vic-ジオールはさらに過剰の過ヨウ素酸による反応で五員環中間体を経て、二つのカルボニル化合物へと酸化開裂されます。
つまり、
・オスミウム触媒の再生
・vic-ジオールの酸化開裂
という
二つの工程が、一つの試薬によって同時に進行します。
その結果、反応容器を変えることなく、アルケンから直接、二つのアルデヒドまたはケトンへと変換するワンポット反応が実現します。
一つの反応容器で複数の化学変換を連続的に進める反応をワンポット反応と言います。
精製操作の少なさや廃棄物の量の観点から重要視されています。
発展経路:過ヨウ素酸でエポキシから直接酸化開裂する
ここまで、vic-ジオールを経由して五員環中間体を形成し、酸化開裂へ至る経路を見てきました。
実は、”過ヨウ素酸”はこの五員環中間体へ「ジオールを作らずに」到達する経路も与えます。
この章では、反応の出発点は異なるものの、途中で同じ中間体に合流し、最終的には同じ機構で説明できる発展的な経路を確認します。
反応機構の全体の流れを確認
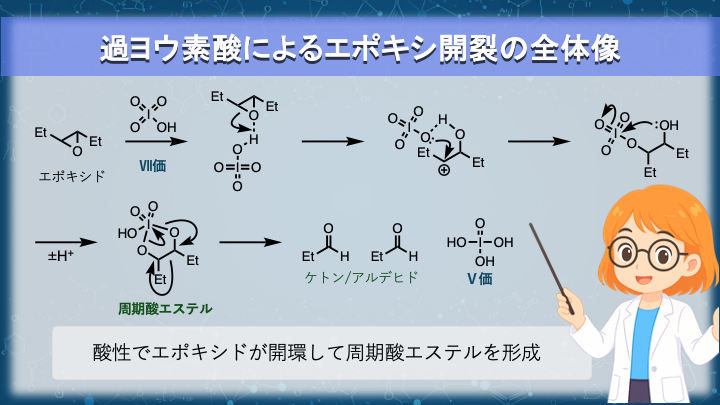
反応機構の全体をまずは俯瞰してみましょう。
- 1. 強酸性条件下でエポキシドが活性化され、開環可能な状態になる。
- 2. エポキシドが開環して、すぐに過ヨウ素酸イオンが付加する。
- 3. 五員環中間体から電子の授受が行われ、ヨウ素はⅦ→Ⅴに酸化数が変化する。
- 4. 二つのカルボニル化合物が遊離する。
過ヨウ素酸は酸性を示すので、酸に弱い官能基が共存する場合はうまくいかないこともあります。
反応機構解説① エポキシの開環
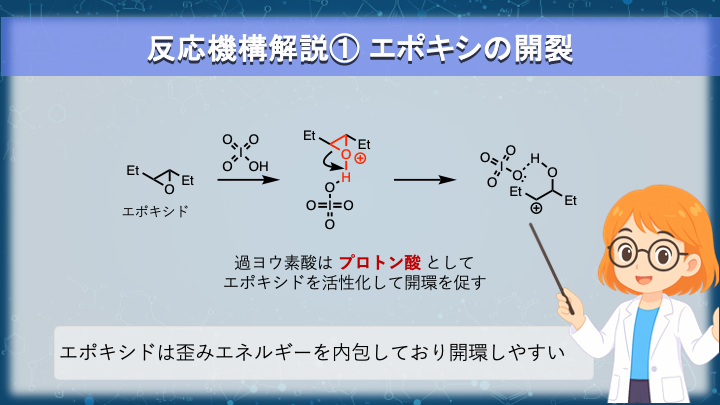
過ヨウ素酸は酸として働き、エポキシドの酸素原子をプロトン化します。
この活性化によって、歪んだ三員環構造は開環しやすくなります。
この段階では、エポキシドの C–O 結合が切れ、求核付加を受け入れる状態が生じます。
反応機構を書く際には、一時的に正電荷を帯びた炭素が生じるように描かれることがありますが、この状態は長く存在するものではありません。
実際には、開環とほぼ同時に過ヨウ素酸イオンの付加が進行し、正電荷は速やかに解消されると考えるのが自然です。
どちらの C–O 結合が切れやすいかについては、正電荷をより安定化できる方向が選ばれると考えられます。
ただし、この後すぐに対称的な五員環中間体へと合流するため、この段階での違いは最終生成物には影響しません。
エポキシの酸性条件での開環、置換については
ブルース11章で取り扱います!
反応機構解説② 過ヨウ素酸の付加
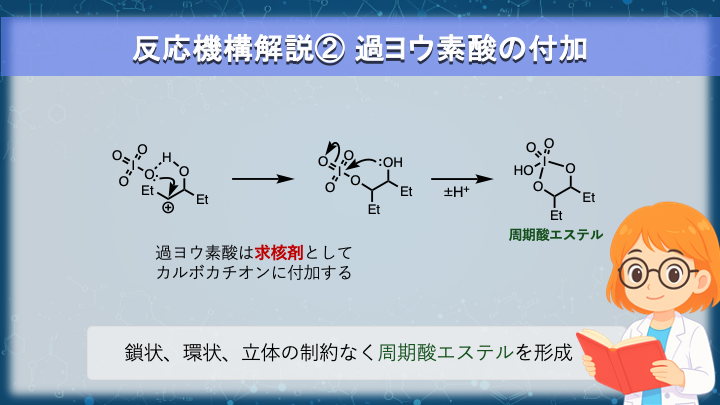
過ヨウ素酸は、最初に酸としてエポキシドを活性化したあと、
そのまま反応系に残り、 次の段階では求核剤として働きます。
エポキシドの開環によって生じた電子不足な炭素原子に向かって、過ヨウ素酸の酸素原子の孤立電子対が求核攻撃して結合を形成します。
付加の結果、基質側には新たな C–O–I 結合が形成され、続いて隣接する水酸基の酸素が ヨウ素中心に結合することで、五員環の周期酸エステル中間体が完成します。
この五員環中間体は、5章で扱った vic-ジオールの酸化開裂反応でも現れたものと本質的に同一です。
したがって経路は異なっても、ここから先の電子の流れは共通になります。
反応機構解説③ 五員環中間体から酸化開裂
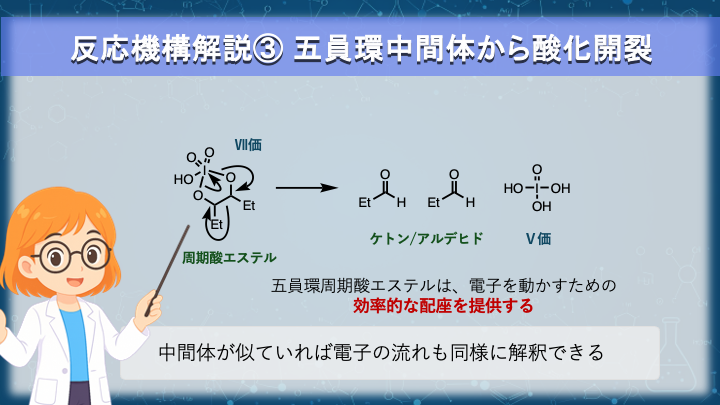
グリコール分解の時の中間体の構造が同じである以上、この先に起こる電子の流れも同じになります。
I–O 結合の開裂とそれに伴う電子移動、C–C 結合の切断によるカルボニル基の形成、
そしてヨウ素のⅦ価からⅤ価への還元は、すべて前章で示した機構に従って進行します。
違いを比較する似ているところを見つける。
全て知識を補強する土台としての思い出になります。
統合:アルケン酸化開裂のルートマップ(#U8含む)
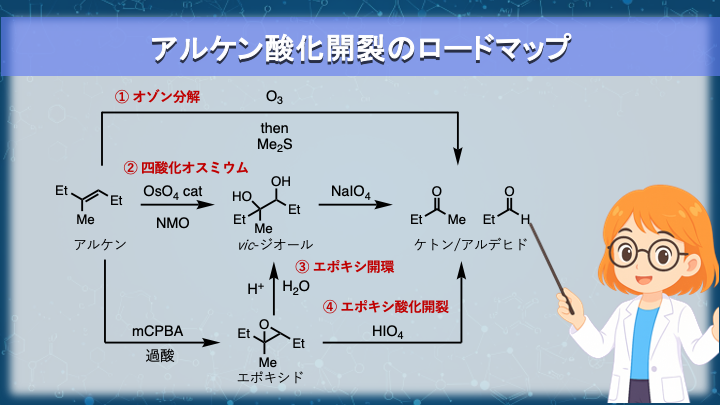
ここまでで、アルケンを二つのカルボニル基に変換するための複数の反応経路を見てきました。
改めて、今回扱った経路を整理してみましょう。
① オゾン分解
→ 強力で汎用的。後処理によって官能基を調整できる。
② OsO₄ →vic-ジオール → NaIO₄
→環状基質にも適用可能。ワンポット化も可能。
③ エポキシ化 → 加水分解 → vic-ジオール → NaIO₄
→ 安価な試薬で実行可能だが、鎖状基質に限定される。
④ エポキシ化 → 過ヨウ素酸による直接開裂
→ 環状基質にも適用できるが、酸に弱い官能基には不向き。
ここで大切なのは、「どの反応が一番優れているか」を決めることではありません。
・基質は環状か、鎖状か
・酸に弱い官能基は含まれていないか
・試薬コストや操作性はどこまで許容できるか
こうした条件によって、“最適な経路”は毎回変わります。
反応を覚えるとは、答えを一つ持つことではなく、選択肢を持ち、状況に応じて選べるようになることです。
まとめ
今回は、アルケンを二つのカルボニル基に酸化開裂させるための複数の反応経路を見てきました。
今回の講義で押さえてほしいポイントをまとめます。
- 四酸化オスミウムはアルケンにシン付加し、 vic-cis-ジオールを与える
- OsO₄ は毒性とコストの観点から、再酸化剤を用いて触媒量で使うのが一般的である
- エポキシは歪みをもったエーテルであり、酸性条件では開環してvic-trans-ジオールを与える
- 過ヨウ素酸はヨウ素のオキソ酸の中で最も高い酸化数をもつ
- vic-ジオールの酸化開裂は、五員環中間体を経由することで進行する
アルケンの酸化開裂には、一つの「正解ルート」があるわけではありません。
正解のルートなんて試してみなければわからないのです。
反応を学ぶとは、答えを一つ覚えることではなく、選択肢を増やし、使い分けられるようになることです。
今回で得た学びが次に新しい分子や反応を前にしたときの思考の出発点になれば嬉しいです。
最後に
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
今回で、ブルース有機化学における「アルケンの求電子反応」については、一通り学習したことになります。
一瞬でしたか?
(そう感じてもらえていたら嬉しいです)
正直なところ、私はそこそこの達成感があります。
学部生相手に授業をすることはあっても、
文章として、資料として体系的に残すのは初めてで、
書くこと・調べることの奥深さに日々、血涙を流しています(笑)
ブルース有機化学の流れに従えば、
次はいよいよアルキンの反応に進みます。
ただ、その前に
・アルケン反応を整理して総復習するルート
・そのままアルキンの反応へ進むルート
どちらも選べるように、現在それぞれ記事を準備中です。
学び方を自分で選べるのも、学ぶことの楽しいところだと思っています。
レベルも、ペースも、興味の持ち方も人それぞれ。
それぞれの角度から、
有機化学に触れてもらえたら、著者としてとても嬉しいです。
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック










コメントを残す コメントをキャンセル