- ジエンとジエノフィルの分子軌道を描くことができる
- どの軌道がHOMOまたは、LUMOなのか考えることができる
- Diels-Alder反応の位置選択性、立体選択性について分子軌道論の考え方と図を用いて説明できる
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に「理解でつなぐ大学有機化学」をかわいくお届けします。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を
今日も一緒に見ていきましょう。
「木を見て森を見ず」という言葉があります。
視野が狭くなると、本質から遠ざかる──
日常の悩みでも勉強でもよくあることですよね。
前回 #U6 では、Diels–Alder反応をできるだけ感覚的にお届けしました。

今回は少し“視点を変えて”、同じ Diels–Alder反応をフロンティア軌道論というレンズで観察しなおします。
本質まで辿り着くのは大変だけれど、乗り越えた先にはきっと一段強くなった自分がいます。
少しは私の言葉に“カンカ”されてやる気が湧いてきました?
aIRaの講義は訪れてくれたすべての学ぶ人に“付加”価値を提供します。
早く、多く『周回すること』の楽しさと『効率の高さ』を感じることができますように
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
Diels-Alder 反応とは
Diels-Alder 反応の重要なポイントまとめ

ここでは、この講義で必ず押さえてほしいポイントを先にまとめておきます。
フロンティア軌道論への第一歩です!安心してついてきてねー
① ジエンのHOMOとジエノフィルのLUMOが相互作用する。
有機反応は最高被占軌道(HOMO)と最低空軌道(LUMO)の重なりで決まる。
② 二つの反応点で結合性相互作用が起こるため、協奏的に2本のC–C結合が形成される。
この“同時性”が、段階的中間体をもたない[4+2]付加環化の本質。
③ 軌道係数が大きい位置同士が最も結合しやすい。
位置選択性は、置換基によって変わる軌道係数(HOMO/LUMO の広がり)で説明できる。
④ HOMO–LUMOギャップが小さいほど反応は速くなる。
電子供与性基はHOMOを上げ、電子求引性基はLUMOを下げることでエネルギー差が縮まる。
⑤ 二次軌道相互作用が endo 体の遷移状態を安定化する。
反応点以外の軌道の重なりが遷移状態に影響し、endo 選択性を生む。
#U6の内容理解に自信がない人は、別タブで開いて一緒に確認しよう
まずはDiels-Alder 反応を一言で説明
#U6を読んでくれた人は復習も多く含まれています。
反応の全体像を先に一文で押さえておくと、
この先の理解がとても楽になります。
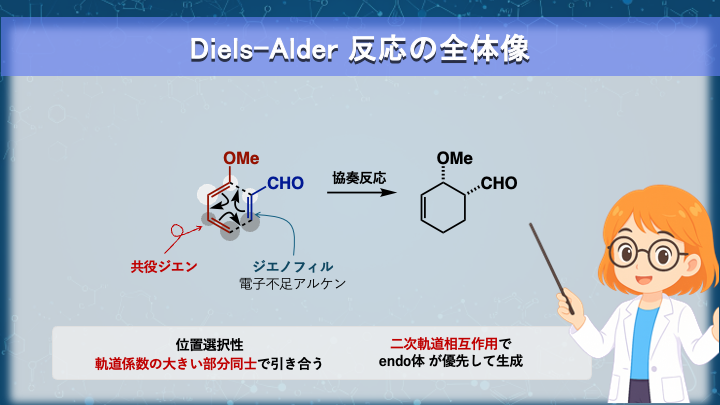
Diels–Alder反応とは、
“共役ジエンの4電子”と“ジエノフィルの2電子”が
ぐるっと環を一周して、協奏的に
6員環(主にシクロヘキセン)を一挙に構築する反応です。
ジエンの4電子、ジエノフィルの2電子が反応に関わることから、
[4+2]付加環化反応と呼ばれています。
弱い3本のπ結合から、
強いσ結合2本+π結合1本へと変わるため、
エネルギー的にも有利な反応です。
熱的な条件で平衡反応になることもあるので、駆動力の理解は大切。
フロンティア軌道論とは

フロンティア軌道論(FMO理論)は、
「反応は HOMO と LUMO の相互作用で決まる」
という、とても強力な考え方です。
反応する二つの分子のうち、
片方の 最高被占軌道(HOMO) と、もう片方の 最低空軌道(LUMO) が
同位相で重なれるかどうか──これが反応の本質です。
HOMO(Highest Occupied Molecular Orbital)
→ 電子が入っている軌道のうち、最もエネルギーが高いもの
LUMO(Lowest Unoccupied Molecular Orbital)
→ 電子が入っていない軌道のうち、最もエネルギーが低いもの
英名・略称・日本語がすべて対応しているので、セットで覚えてしまうのがおすすめ。
そしてこれは Diels–Alder反応だけの話ではありません。
ほとんどすべての有機反応は、
HOMO(=求核剤の軌道)から
LUMO(=求電子剤の軌道)へ
電子が移動することで理解できます。
求核剤と求電子剤がなぜ反応するのか、どこで反応するのかを軌道の形で解釈するのがフロンティア軌道論です。
① ジエンのHOMOとジエノフィルのLUMOが相互作用する。
Diels–Alder反応の本質は、ジエンのHOMO と ジエノフィルのLUMO が、
「両方の反応点で同位相で重なれるかどうか」にあります。
まず、エチレンとブタジエンを例に、軌道の形を目で確認していきましょう。
ジエンのHOMOとLUMOはどのような軌道か
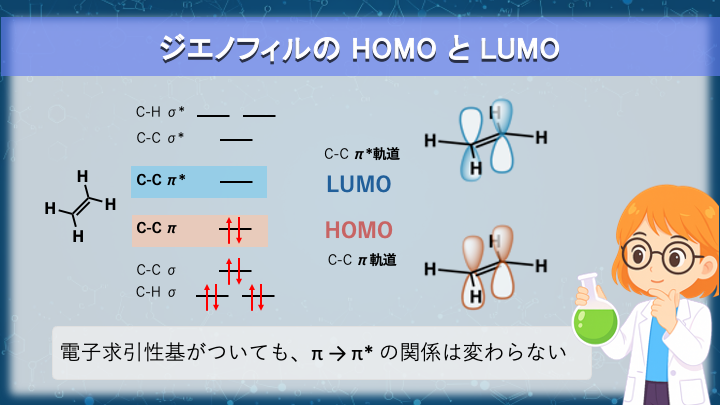
エチレンの分子軌道は、エネルギーの低い順に
C–H σ ×4 → C–C σ → C–C π → C–C π* → C–C σ* → C–H σ* ×4
と並びます。
電子が埋まっているのは π 軌道までなので、
- HOMO:C–C π
- LUMO:C–C π*
となります。
直接の重なりで作られるσ軌道とふわっとした重なりで作られるπ軌道のどちらが高エネルギーか説明できるかな?
ジエノフィルのHOMOとLUMOはどのような軌道か
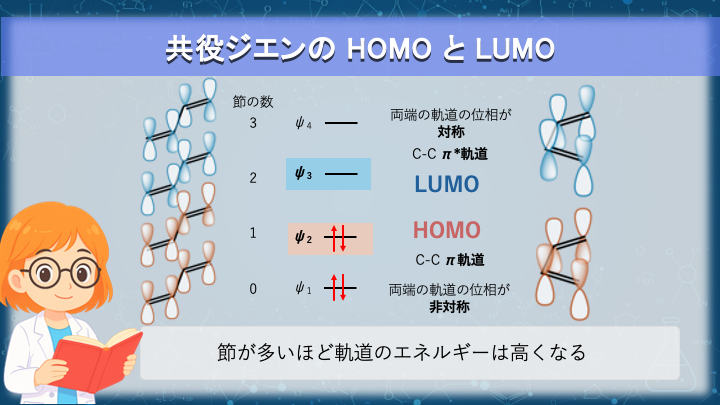
4つの炭素が直列に並んだブタジエンでは、
4つの p 軌道が相互作用して、
4つの分子軌道(ψ₁〜ψ₄) が生成します。
分子軌道のエネルギーは「節(ノード)」の数で決まります。
- ψ₁:節 0(最安定)
- ψ₂:節 1(HOMO)
- ψ₃:節 2(LUMO)
- ψ₄:節 3(最高不安定)
4電子が入るので、
HOMO は ψ₂、LUMO は ψ₃ になります。
HOMO(ψ₂)は両端の符号が異なるため非対称になり、
LUMO(ψ₃)は両端が同じ符号のため対称性が高い軌道になります。
初学者はすべてを覚える必要はありません。
まずは ψ₂(HOMO)が“非対称”だという事実を基軸に理解すると良いと思います!
私は5周目くらいでやっとわかって、説明するのに7周くらい考え直した。。。
分からなくても大丈夫。とりあえず進んで、何度も戻って考え直してみよう。
軌道支配な反応は同相な軌道の相互作用により進行する
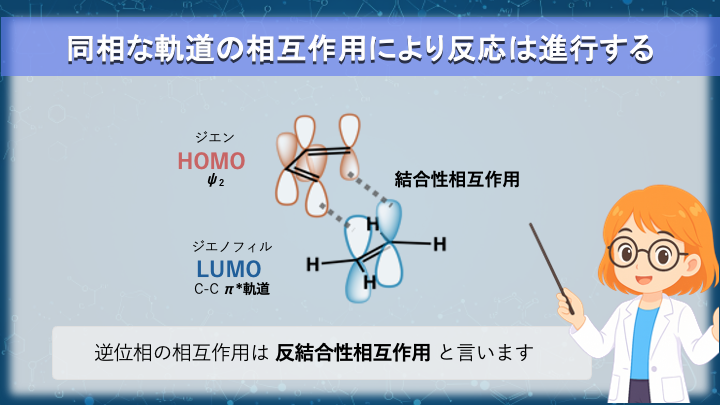
フロンティア軌道論では、反応の鍵は
軌道どうしの結合性相互作用(同位相の重なり) にあります。
効果的な軌道相互作用の条件は 2 つ。
① 一方が被占軌道(HOMO)、もう一方が空軌道(LUMO)であること。
被占同士では電子反発が起こり、結合性の相互作用にはなりません。
② 反応点で“同位相”として重なれること。
同位相 → 結合性相互作用を形成
逆位相 → 半結合性(反結合性)になり結合を弱める
Diels–Alder反応では、
ジエンの HOMO(ψ₂) とジエノフィルの LUMO(π*) が
両方の反応点で同位相として重なれる ため、
協奏的に 2 本の新しい C–C 結合が同時に形成されます。
これに対して、熱的 [2+2] 付加は、
2 点のうち片方で必ず逆位相となるため、
対称性の理由から進行できません(Woodward–Hoffmann則)。
② 二つの反応点で結合性相互作用が起こるため、 協奏的に2本の C–C 結合が形成される
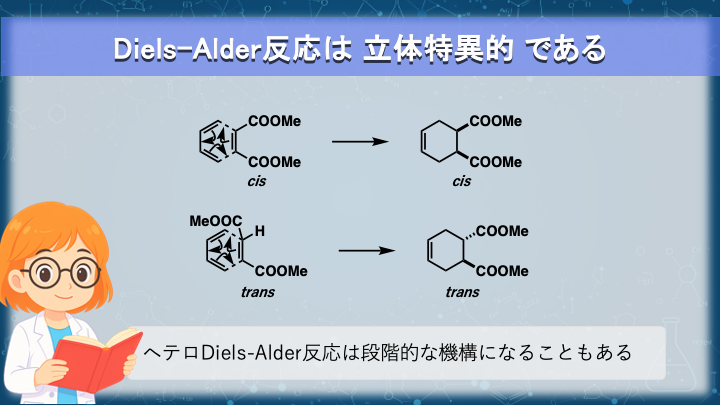
Diels–Alder反応では、
ジエンとジエノフィルの 2つの反応点が同時に結合性相互作用をとれる
という特徴があります。
両方の点で軌道が 同位相かつ同程度に重なれる ため、
2本の C–C 結合が“一挙に”形成される=協奏的 になります。
協奏的で中間体を経ない反応なので、
出発物質の E/Z などの幾何異性はそのまま生成物に写し取られます。
なお、反応点どうしの軌道係数が極端に不均一な場合には、
付加環化が段階的に進む(ヘテロDiels–Alder)例もありますが、
これは例外的なケースです。
③ “軌道係数が大きい位置同士”が最も結合しやすい。
位置選択性は、結局のところ
「分子軌道がどの位置にどれだけ広がっているか」 で決まります。
この“広がり”を表す指標が 軌道係数 です。
軌道係数とは、分子軌道をつくる際に
各 p 軌道がどれだけ寄与しているかを示す数字で、
係数が大きいほど、その位置の軌道は“山が大きく、高く”広がっていると考えられます。
したがって、
HOMO(求核側)で軌道係数の大きい位置 と
LUMO(求電子側)で軌道係数の大きい位置 が
最も効率よく重なり、結合しやすくなります。
置換基は、この軌道係数の大きさを変化させ、
どの位置がより反応しやすいかを決める要因になります。
詳しくは次節で扱います。
置換基は軌道係数をどう変えるか
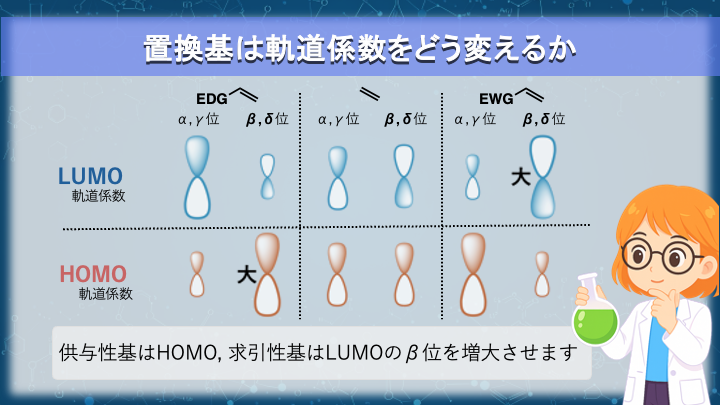
置換基は、分子軌道そのものの“形”をゆがませる力を持っています。
電子を押し出す基(電子供与性基)なら軌道を外側へふくらませ、
電子を引き込む基(電子求引性基)なら軌道を内側へ引き寄せます。
この“ゆがみ”は、特に 置換基の隣の炭素(β位〜δ位) の軌道係数に反映されます。
- 電子供与性基 EDG (OR、NR₂、アルキルなど)
→ HOMO の β位の軌道係数を増大させ、求核性を高めます。 - 電子求引性基 EWG (CN、NO₂、CO₂R など)
→ LUMO の β位の軌道係数を増大させ、求電子性を高めます。
フロンティア軌道論では“どこが電子豊富か/不足か”を
**軌道の広がり(係数)**として読み取ることで、
位置選択性をより本質的に理解できます。
軌道係数の大きい同士で結合は形成される
では、実際に“どこ同士が結合するのか”を軌道で読み取ってみましょう。
例として 2-メトキシ-1,3-ブタジエン と アクリロニトリル を並べます。
図では、円の大きさがその位置の 軌道係数(広がり)、
円の色が 位相 を示しています。
- アクリロニトリルの CN 基 は、LUMO の β位 の軌道係数を強く大きくする
- メトキシ基(OMe)は、HOMO の β位 の軌道係数を大きくする
つまり、
「最も広がった同位相のペア」
=「最も結合しやすい反応点」
というわけです。
#U6 では電荷のかたよりとして説明しましたが、
フロンティア軌道論では“なぜその位置が電子豊富/不足になるのか”を
軌道の形そのもの から読めるようになります。
これは一度理解するととても強力で、
求核置換・求電子置換・付加,脱離機構まで、
ほとんどの反応に応用できます。
④ HOMO–LUMO ギャップが減少すると反応速度が向上する。
ここまでの議論では、軌道係数(軌道の“広がり”)を使って
「どこが結合するか」(位置選択性)を説明してきました。
一方で、「どれくらい速く反応が進むか」は、
相互作用する軌道のエネルギー差で決まってきます。
フロンティア軌道論の視点では、
ジエンの HOMO とジエノフィルの LUMO のエネルギー差が小さいほど、
二つの軌道が強く混成し、
遷移状態がより安定化する → 活性化エネルギーが下がる → 反応が速くなる
という流れで理解することができます。
Diels–Alder反応においては、
この HOMO–LUMO ギャップがまさに
「反応の起こりやすさ」を測る指標になります。
#U6 では経験的に「置換基が反応速度を変える」と見てきました。
ここでは、その置換基効果を HOMO と LUMO のエネルギー操作としてとらえ直し、
Diels–Alder反応の“速さの理由”をもう一段深く掘り下げていきましょう。
置換基は軌道エネルギーをどう変えるか
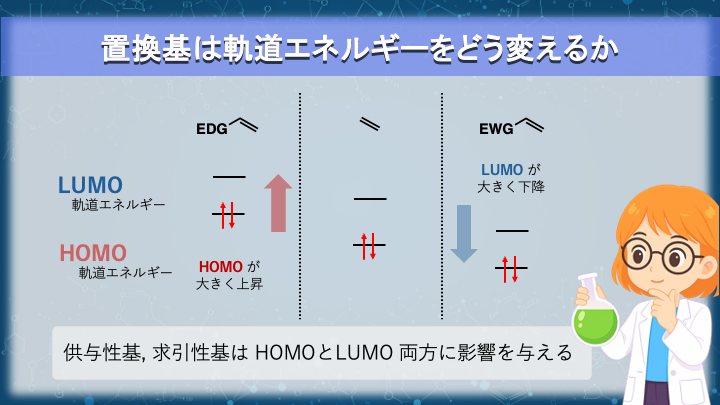
置換基は、分子軌道の“エネルギー準位”に影響します。
電子供与性基(OR、NR₂、アルキル)は軌道エネルギーを押し上げ、
電子求引性基(CN、NO₂、CO₂R)は軌道エネルギーを引き下げます。
特に重要なのは、
電子供与性基 は HOMO を強く上昇させ、
電子求引性基 は LUMO を強く下降させる という点です。
HOMO–LUMO のエネルギー差が縮まると、
両軌道の相互作用がより効率的に起こり、
遷移状態が安定化して反応が加速されます。
Diels–Alder反応では、
「ジエンに電子供与性基」「ジエノフィルに電子求引性基」
という組み合わせが特に反応性を高める理由は、
まさにこのエネルギーギャップの縮小にあります。
HOMOとLUMOのエネルギー差が小さいと反応はより効率的になる
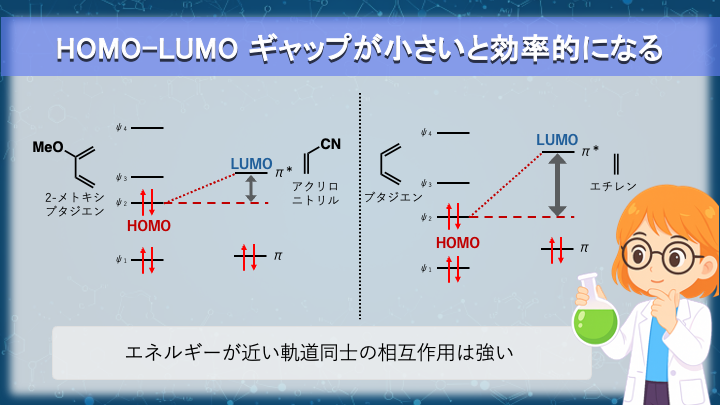
では、置換基によるエネルギー調節が実際の反応性にどうつながるのか、
代表例で読み解いてみましょう。
比較するのは次の 2 系列です。
- 2-メトキシ-1,3-ブタジエン × アクリロニトリル
- ブタジエン × エチレン
共役ジエンには 4 つの π 軌道(ψ1〜ψ4)があり、HOMO は ψ2 に該当します。
メトキシ基(電子供与性基)が結合すると、この HOMO のエネルギーが押し上げられます。
ジエノフィル側では、LUMO は π* 軌道に当たります。
アクリロニトリル(CN基)は強い電子求引性基であり、π* 軌道のエネルギーを引き下げます。
その結果、
HOMO(ジエン)↑ と
LUMO(ジエノフィル)↓ の両方が起こり、
HOMO–LUMO ギャップが大きく縮まる。
エネルギーギャップが縮まると、
両軌道の相互作用が強くなり、
遷移状態がより大きく安定化し、
付加環化反応は顕著に加速します。
つまり、
供与性基-ジエン × 求引性基-ジエノフィル
の組み合わせは圧倒的に速い Diels–Alder 反応を与えます。
⑤ 二次軌道相互作用が endo 体の遷移状態を安定化する。
#U6 では、ジエンとジエノフィルが「分子全体で引き合う」ために endo 体が優先する、と説明しました。
そのときの表現は、あくまで“現象としての説明”でした。
フロンティア軌道論の視点を手に入れた今なら、
その「分子全体で引き合う」という現象が、どんな軌道同士の相互作用から生まれるのか
をより精密に理解できます。
鍵になるのが 二次軌道相互作用 です。
これは、結合が形成される“反応点以外”でも、HOMO と LUMO が同位相で重なり、
遷移状態を追加で安定化する相互作用のことです。
ここでは、メチルビニルケトンとシクロペンタジエンを例に、
ジエノフィル側の LUMO がどのように分子全体へ広がり、
なぜ endo 体でだけ追加の安定化が生じるのかを見ていきましょう。
ジエノフィルのLUMOを広く観察する

反応点だけを見ると、ジエノフィルは単なる C=C の π 軌道と π* 軌道のように思えます。
しかし endo 則の本質は、反応点“以外”の部分にも LUMO が広がっている点 にあります。
そこでジエノフィル全体の LUMO を、少し引いた視点で眺めてみましょう。
メチルビニルケトンでは、C=C の両端の p 軌道に加えて、
カルボニル基の炭素と酸素の p 軌道も LUMO の形成に参加します。
結果として 4 つの p 軌道が組み合わさり、節の数が 0〜3 の 4 つの分子軌道(ψ1〜ψ4)ができます。
このうち、LUMO に相当する ψ3 は、
“カルボニル方向へ大きく広がったLUMO” になっているのが重要点です。
この広がりこそが、のちの二次軌道相互作用につながります
反応点以外の軌道の相互作用を二次軌道相互作用という
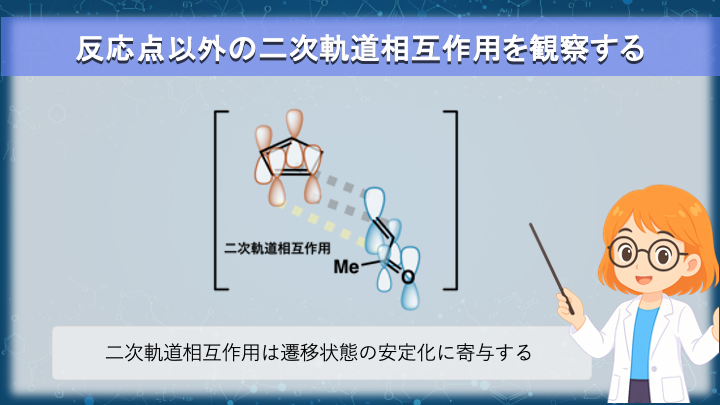
endo 体と exo 体の遷移状態を見比べると、どちらも反応点では
HOMO と LUMO が同位相で重なる
という点は共通しています。
しかし endo 遷移状態では、反応点以外にも着目できます。
メチルビニルケトンの LUMO は、C=C の端だけでなく
カルボニル方向へも大きく振幅が広がって います。
この広がった部分が、シクロペンタジエンの HOMO の末端部分と
同位相で追加の重なりを作れる のがポイントです。
このように、
「結合ができる位置“以外”で生じる HOMO–LUMO の同位相重なり」
を 二次軌道相互作用(secondary orbital interaction) と呼びます。
この追加の安定化が endo 遷移状態のエネルギーを下げ、
結果として endo 体が優先して生成されます。
まとめ
① ジエンのHOMOとジエノフィルのLUMOが相互作用する。
有機反応は最高被占軌道(HOMO)と最低空軌道(LUMO)の重なりで決まる。
② 二つの反応点で結合性相互作用が起こるため、協奏的に2本のC–C結合が形成される
協奏的ゆえにジエンとジエノフィルの幾何異性は反映される。
③ 軌道係数が大きい位置同士が最も結合しやすい
置換基は軌道の形を歪め、広がりの大きい部分と小さい部分を作る。
④ HOMO–LUMOギャップが小さいほど反応は速くなる
エネルギーギャップが縮まると、両軌道の相互作用が強くなり、反応が加速される。
⑤ 二次軌道相互作用が endo 体の遷移状態を安定化する
反応点以外の軌道の重なりが遷移状態に影響し、endo 選択性を生む。
最後に
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
#U1 から追ってくれている学生さん、今回の内容はなかなかの強敵だったはず。
でもね、フロンティア軌道論のレンズで世界が“色づいて”に見えてきたら、もう立派な中級者だよ!
もっと深く知りたい人には、私のお気に入りの専門書たちもおすすめです。
いずれ紹介したらリンク貼っておきますね!
次回は、Diels–Alder の親戚、“1,3-双極付加環化反応”を扱います。
アルケンがケトンに“スパッ”と割れる、大学入試でもおなじみのあの反応。
さらに、実験する側だからこそ知っておきたい“危険性”もお話しする予定です。
楽しい実験でも、安全でないなら……
オオゾンしてしまいますからね。
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック











コメントを残す コメントをキャンセル