- ヒドロホウ素化酸化の反応全体像と電子の流れを説明できる。
- ヒドロホウ素化がアンチマルコフニコフ付加となる理由を説明できる。
- 代表的なホウ素化試薬の種類と特徴を例示できる。
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に「理解でつなぐ大学有機化学」をかわいくお届けします。
🌸 導入

やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
『ヒドロホウ素化酸化反応』で副生するホウ酸 B(OH)3 が、ゴキブリ退治で大活躍なことはみんな知っているけど、ホウ素の化学に詳しい人って限られてくるよね!
8電子を満たしていないからこそ、初学者にはちょっと難しいホウ素の反応も、
マルコフニコフ則に反抗する理由も、
この講義を見れば、だれでも図で理解することができます!
『ヒドロホウ素化酸化』は苦手な人も多いけれど、大学院入試や国家試験では頻出。
「あのケアレスミス、ちゃんと理解していれば防げたかも…」なんて経験、ありませんか?
この記事でホウ素の化学を一つずつ整理して、他の反応にも応用できる力をつけましょう!
アルケンの反応はマルコフニコフ則で完璧だって?
もちろん俺らは抵抗するで!ホウ素で!👊
……それじゃ、始めましょう!(〃 ̄ω ̄〃ゞ💦
👀 (1) ヒドロホウ素化酸化を一言で
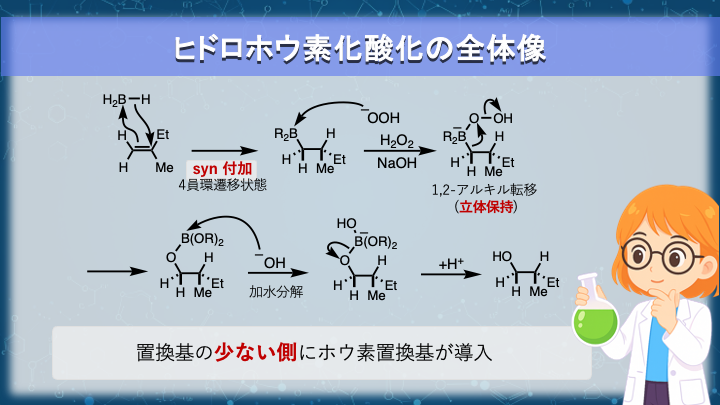
まずは全体像を確認して自分がどこまで説明できるか、振り返ってみましょう。
アルケンに BH3 が同じ面から付加(ヒドロホウ素化)し、その後 H2O2/NaOH で酸化してアルコールに変換する反応です。
一行スキーム:
C=C → (BH3,syn 付加) → R–CH2–CH2–B(…)
→ (H2O2/NaOH) → R–CH2–CH2–OH + B(OH)3
ボランは理論上3当量までのアルケンと反応してトリアルキルボランになります。(条件次第)
酸化段階の要点:
塩基下で生じる HOO−(過酸化物イオン)がホウ素へ求核攻撃して、ボロネートの過酸化物中間体になる。
O–O結合が切断すると同時に B–C のσ結合が酸素へ「1–2アルキル転位」する。
この置換は B 上の3本の B–C すべてで起こるので、BH3 1当量で最大アルケン 3当量をアルコールに変換できます。
最後はホウ酸エステル B(OR)3 の加水分解で R–OH に置換されます。
キーワード:
- 機構:協奏的な syn 付加(カチオンもラジカルも経ない)
- 選択性:アンチマルコフニコフ則(OH は置換の少ない炭素側)
- 酸化:HOO− の求核 → O–O切断 + σ結合移動 → B(OR)3 → 加水分解
要点を読んで反応機構が自力で説明できる人は素晴らしい。
実際に問題を解いてみましょう!
「いまの説明、専門用語が多くてわからん…」と感じた人も大丈夫。そんな人に向けて丁寧に説明しますよ!
🧠 (2) 反応機構を丁寧に考える
⚡️ (2-0) ボランの反応性を理解
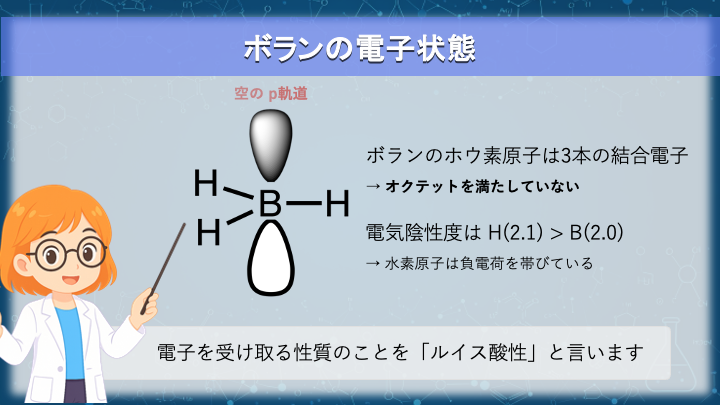
まずは唐突に出てきたボラン(BH3)という化合物について丁寧に解説します。
ホウ素原子に3つの水素原子が結合しています。ホウ素は13族元素なので、3本の共有結合をつくると中性の状態になりますね。
しかし、ボランのホウ素原子は孤立電子対を持たないため、ホウ素の周囲に6電子しかありません。
原子は通常、最外殻に8電子(オクテット)あると安定です。したがって、ボランは2電子分の“空き”を抱えていることになります。
原子軌道論的に整理すると、ボランのホウ素原子は反応性の空の p 軌道を持っているという解釈になります。
このように電子を受け取る性質を、大学では「ルイス酸性」と呼びます。
ルイス酸性の高い分子は、ヘテロ原子の孤立電子対やアルケン・アルキンの π 電子と引き合い、配位結合をしたり相互作用を起点に求電子剤として反応に関わったりします。
また、電気陰性度を比較すると B ≈ 2.0、H ≈ 2.1 なので、B–H はホウ素側が正、水素側が負に分極しています。
つまり、ボランの水素は特定の条件下で還元力を持つということです。
その特定の条件下とは、ホウ素が何かと配位している時です。ホウ素に電子が入り込める環境でのみ、ボランは還元剤として働きます。
ここまでで、ホウ素の反応性、電子的環境を理解できたでしょうか?
少しわかった気がした人は、実際の反応機構を丁寧に確認していきましょう。
電子対を受け取って四面体のボレートになると、オクテットは満たすんだけど、今度は電子が多いなって感じて、ヒドリドやアルキル基を押し出したくなっちゃう。贅沢なやつだな!
✏️ (2-1) 反応機構① 協奏的な付加(ヒドロホウ素化)
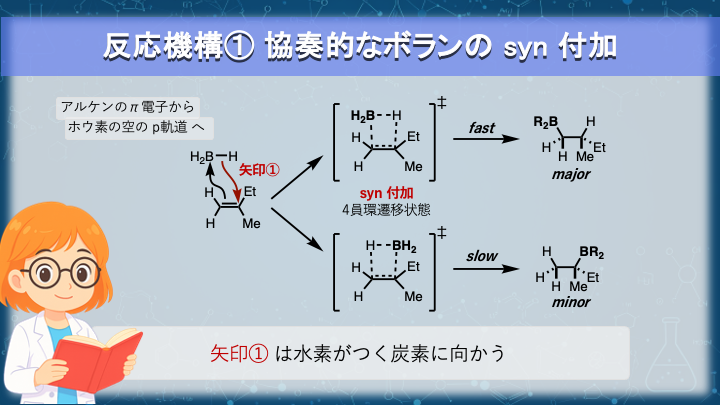
ヒドロホウ素化の第一段階は、アルケンとボランの協奏的な付加です。
アルケンの π 電子が電子不足なホウ素へ流れ、同時に B–H 結合の σ 電子が反対側の炭素に移動します。
その結果、C–B 結合と C–H 結合が同時に生成します。
この反応では、電子の動きがすべて同時に進むため、カルボカチオンのような中間体は存在しません。つまり、転位反応が起こらないということですね。
反応は四員環の遷移状態を経て進行し、水素とホウ素は同じ面から導入されます(syn 付加)。
ボランには3本の B–H 結合があり、1分子の BH3 から最大3分子のアルケンと反応します。
反応が進むと、モノ・ジ・トリアルキルボランの混合物が得られます。生成比はアルケンの構造や反応条件によって変化しますが、ここでは詳しく触れません。
この反応で一番注目すべきなのは、「ホウ素がどの炭素に結合するのか」という位置選択性です。
付加の結果、ホウ素はより置換基の少ない炭素に結合します。
これは、置換基の多い炭素に新しい置換基が導入されるというマルコフニコフ則とは真逆の傾向。
いわゆる「アンチマルコフニコフ則」と呼ばれる付加ですね!
ヒドロホウ素化では、このアンチマルコフニコフ付加が必ず登場します。もちろん、この講義では暗記で終わらせません!
なぜこうなるのか、理由とセットで理解することが本当の基礎です。次は、なぜアンチマルコフニコフ則に従うのかを見ていきましょう。
協奏反応、syn 付加の意味を復習したい人は #U3「協奏する分子」をチェック!👊
💡 (2-2) なぜアンチマルコフニコフ則になるのか?(立体効果)
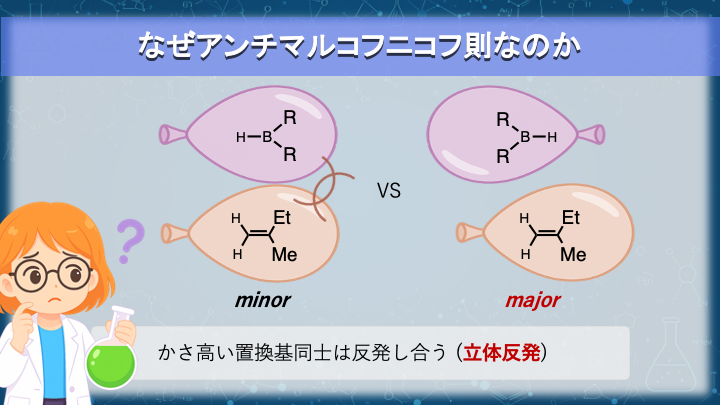
ここが、ヒドロホウ素化でいちばん重要な部分です。
なぜホウ素は“置換基の少ない炭素”を選ぶのでしょうか?
その理由は、分子同士の立体的な押し合いにあります。
ホウ素試薬は電子を受け取りたがる一方で、自分のまわりも少し混み合っています。だから、できるだけぶつからない方向からアルケンに近づこうとするのですね。
アルケンの炭素も、置換基が多いほど周囲がかさばっています。結果として、ホウ素は自然と“すいている”=置換基の少ない炭素を選ぶのです。
この傾向は、使う試薬によっても変わります。アルキルボラン(RBH2、R2BH など)のように、大きい試薬ほど立体障害の影響が強まり、位置選択性がよりはっきりと現れます。
水風船を近づけるイメージと同じで、かさ高い部位同士は弾かれます。したがって、B は混み合っていない=置換の少ない炭素側から入りやすいです。
複雑な分子で立体障害を考えるときは、試薬がどんな角度や方向から近づくかをイメージするのも大事になったりしますね!
この立体障害の考え方は、ヒドロホウ素化だけでなく、ほかの反応の位置選択性や立体選択性を理解するうえでも欠かせません。しっかり押さえておきましょう。
✏️ (2-3) 反応機構② 過酸化物イオンの付加
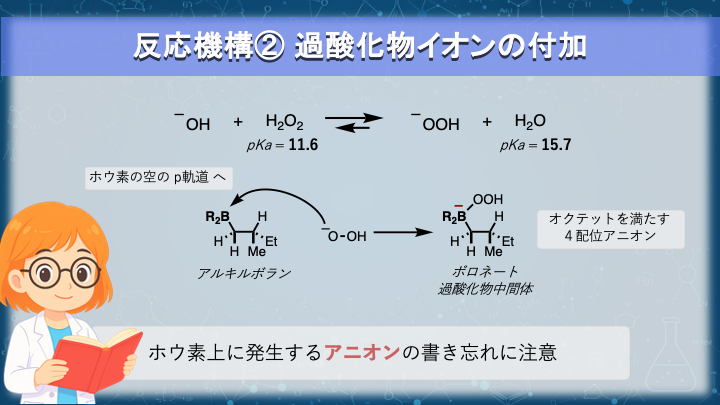
ヒドロホウ素化で生成したアルキルボランは、そのままでは安定な生成物です。
ここに過酸化水素と水酸化ナトリウムを加えると、酸化的条件下でホウ素をヒドロキシ基に置き換える反応が進行します。
塩基は過酸化水素を脱プロトン化し、求核性の高い過酸化物イオン HOO− を生成します。
一方、アルキルボランのホウ素は空の p 軌道をもつ求電子中心です。
したがって、反応の主経路は HOO− がホウ素を求核攻撃する経路となります。
この段階でホウ素上に形式負電荷がある、ボロネート過酸化物中間体が生成します。この中間体から次にアルキル転位へと続いていきます。
過酸化物イオンは“α効果”と呼ばれる性質で、見かけ以上に強い求核性を示すんです。少し発展的でわかる人はすごいと思います! 詳しくは #A で取り上げますね!
✏️ (2-4) 反応機構③ O–O結合切断とアルキル転位
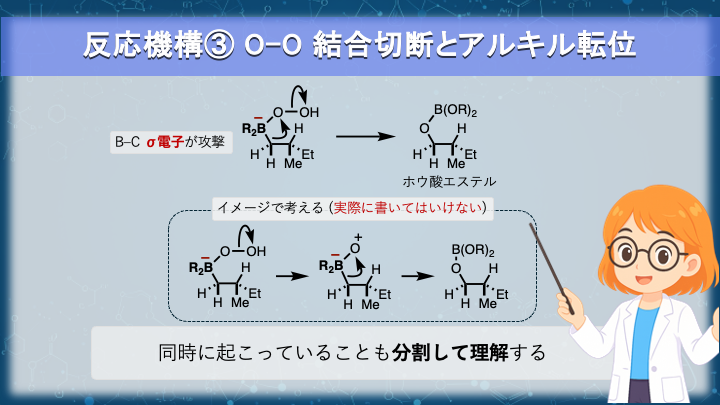
ボロネート中間体ができたあと、反応は次のステップに進みます。ここで起こるのは、O–O結合の切断と、ホウ素上のアルキル基の転位です。
酸素–酸素結合は結合エネルギーが低く、切れやすい結合として知られています。そのため、O–O結合が切れながら、ホウ素に結合していたアルキル基が酸素に移動していきます。
転位が起こるとき、もしそのアルキル基がキラル中心を含んでいれば、立体保持 (retention) のまま転位します。
この転位の反応機構は私自身、初学者の頃に繰り返し間違えましたし、ピンと来なかった電子の流れです。私が理解するために掴んだコツとして、頭の中で電子の流れをスローモーション再生してみましょう。
まず、過酸化物の O–O 結合は切れたがっています。仮に末端の OH が水酸化物イオンとして脱離すると、ホウ素とつながっている酸素には一時的に正電荷が生じることになります。これは、電気陰性度の高い酸素がプラスを抱える“非常に不安定な状態”です。
その不安定さを解消するために、隣のアルキル基が電子対ごと酸素へ移動します。こうして、B–C結合の電子が O–O 結合の切断と連動して動き、アルキル基が転位するのです。
不安定なカチオンから転位が進行して安定化するイメージは、カルボカチオン転位と似ていると感じますが、正電荷が中間体として発生しているわけではないという大きな違いもありますね!
電子の動きを“スロー再生”で追うと、どの結合が切れたいか、どこに電子が流れたいかが一気に見えてきますよ!
ただし、この考え方で大事なのは──この“スローモーションで理解”はあくまでわかりやすく整理するための分割だということです。
実際の反応は、これらの過程(水酸化物の脱離・正電荷の発生・アルキル転位)が同時に起こる反応なのです。つまり、段階的にこれが起こらずに、同時に起こらなければならない理由もまた、しっかりと理解する必要があるのです。
酸素に正電荷の中間体を描いてしまうと、テストでは減点されてしまいます。
✏️ (2-5) 反応機構④ 加水分解によるアルコール生成
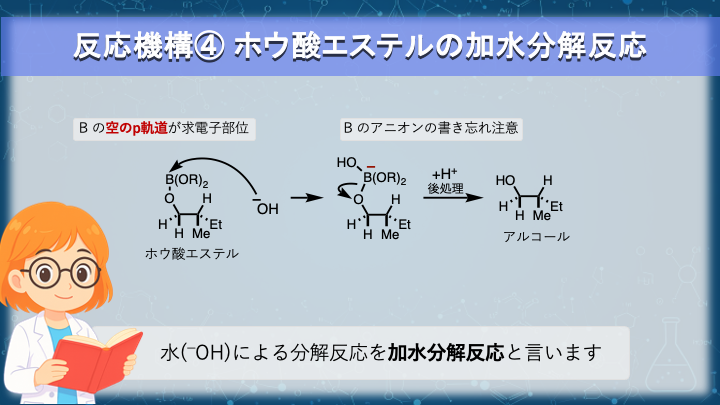
アルキル転位が完了した段階で、分子はボレート(B–OR を3本もつ、いわばホウ酸エステル/トリアルキルボレート)になっています。
ここからは“エステルらしい”化学:水(塩基性)で加水分解して ROH を取り出す段階です。塩基条件では、HO− がホウ素原子へ求核付加 → 四配位ボレート([B(OR)3OH]−)を経由し、アルコール部分が脱離して R–O− が生じます。
フラスコ内が塩基性なら生成直後は R–O−(アルコキシド)、後処理(中和/水洗)で R–OH になります。ホウ素側は加水分解が進み、最終的に B(OH)3(ホウ酸)へ。
ここで押さえたい要点は二つ。
- 場は「ホウ素上での付加–脱離」で進む。
- 反応全体としては、炭素側に新たな C–O 結合ができており“酸化”されている。
カルボン酸エステルの加水分解とは機構は違いますが、どちらも“付加と脱離”で整理できる点ではつながっています。なんか似てない? 体系的に見ると、化学がどんどんシンプルになりますよね✨
💡 (2-6) 反応機構まとめ
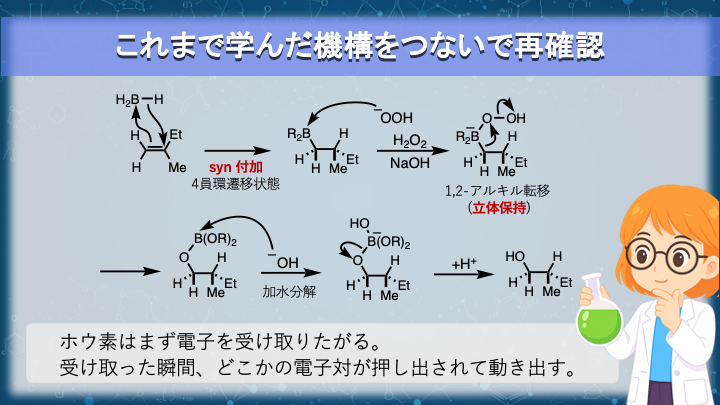
反応機構を丁寧に見終わったので、再度全体を振り返りましょう。ヒドロホウ素化酸化は、次の3段階で進みます:
- ヒドロホウ素化:アルケンが BH3 に協奏的な付加(ホウ素の空軌道と π 電子が同時に反応)。
- 過酸化物酸化:HOO− が求核攻撃 → O–O 結合開裂とアルキル転位。
- 加水分解:ボレートが加水分解され、アルコールとホウ酸を生成。
キーワードを整理すると:
- ヒドロホウ素化は協奏的 syn 付加/4員環遷移状態
- 反マルコフニコフ則(B → 置換少ない側 = OH も同側)
- アルキル転位は立体保持
反応機構の電子の矢印を一つ一つ、どうしてそう流れるのか理解して、再度全体を通して見直す。ヒドロホウ素化酸化の反応機構がどんなに複雑に見えても、丁寧に理解した一つ一つを唱えながら書けば、確実な暗記としっかりとした定着につながります。
⚠️ (2-7) 試験で落としがちなポイントと注意点
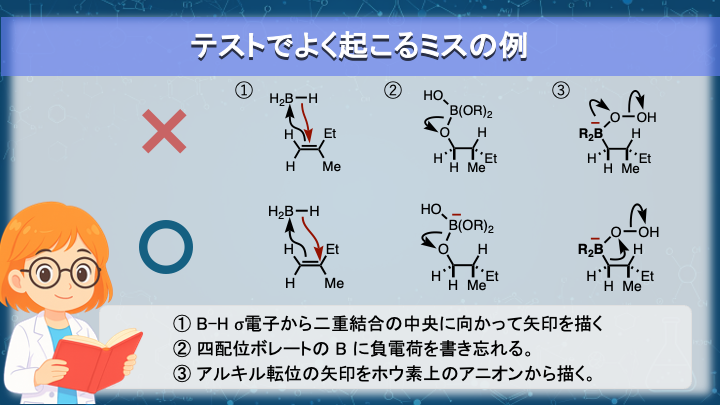
最後に、大学試験や院試で本当に多いミスをまとめます。生成物の構造が完璧でも、ここを落とすと減点されます。
-
B–H σ 電子から二重結合の中央に向かって矢印を描く。
→ ヒドリドが向かう先をしっかりと示すために、この矢印は水素と結合を作る炭素に向かって矢印を描きます。 -
四配位ボレートの B に負電荷を書き忘れる。
→ 反応では電荷は保存。HOO− が入れば、その負電荷は次の構造にも反映される(B に負電荷を明示)。 -
アルキル転位の矢印をホウ素上のアニオンから描く。
→ このアルキル転位は B–C σ 電子が求核本体。アニオンから動かしたら、4本のうちどの結合が動くのか指定できていません。アニオンから動かしていい場合は、その本体が孤立電子対である場合です。
反応機構は“写経”ではなく、「電子がなぜそこに動くのか?」を常に説明できる形で書く。それができれば、初見の機構でも自力で組み立てられますよ。
🌿 (3) 実はボランだけじゃない。いろんなホウ素試薬
ヒドロホウ素化の章では、立体障害が反応の位置選択性を決めると説明しました。つまり、ホウ素まわりの“かさの大きさ”が、どの炭素に結合するかを左右します。
使うホウ素化試薬を変えるだけで、選択性をコントロールすることができます。ここからは、反応性や立体障害のバランスが異なるホウ素試薬をいくつか紹介していきます。
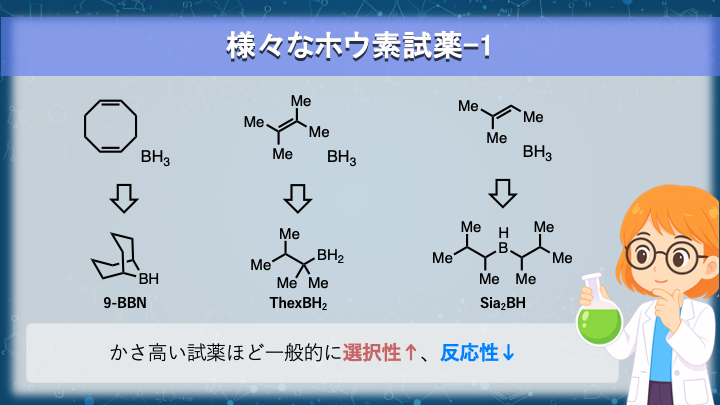
⭐️ (3-1) 9-BBN ― 嵩高いホウ素化試薬代表
9-BBN(9-borabicyclo[3.3.1]nonane)は、ボラン(BH3)をシクロオクタジエンに取り込ませて得られる安定で立体的にかさ高いボラン試薬です。
反応によってホウ素が炭素骨格の内部に組み込まれ、剛直な「ボラビシクロ構造」をつくるため、THF溶液中でも分解しにくく、実験室で最もよく使われる安定ボランの一つになっています。
この “9-borabicyclo[3.3.1]nonane” という名前自体が IUPAC 命名法の良い教材で、骨格番号の付け方や「bora-」の位置関係を考える練習にもなります(詳しくは #B2 で解説予定)。
👉 命名法や詳しい特性を解説しつつ、私が見る構造の美しさを共有したい!
#B2 「9-BBNが最近話題の宇宙人に似ている件」
有機化学を学ぶなら、構造式と正式名称の両方をスラスラ書けるようになっておきたい定番試薬ですね。
9-BBNを美しく描けるようになりたい。かっこよく書くことを目指せば構造を覚えるなんて通過点だね!
(3-2) テキシルボラン ThxBH₂
9-BBN ほど嵩高くはないけれど、反応性と選択性のバランスが良く、扱いやすいのがこのテキシルボラン(ThxBH2, thexylborane, 1,1,2-trimethylpropylborane)です。
この試薬は 2,3-ジメチル-2-ブテンにボラン(BH3)を付加させて調製されます。ここで登場する「テキシル(thexyl)」という名前、少し不思議ですよね。由来とセットで覚えましょう。
ホウ素に結合しているアルキル基が tert-isohexyl 基だから thexyl という名前なのです。
“iso”は末端が二股に分かれた構造、“tert”は官能基がつく炭素が3級(tertiary)ってことだよ。
テキシルボランは B–H 結合を二つ残しているため、1分子の ThxBH2 が2分子のアルケンと反応できます。反応性が高い小さなアルケンの位置選択的ヒドロホウ素化に向いています。
(3-3) ジシアミルボラン Sia₂BH
ジシアミルボラン(disiamylborane, Sia2BH, bis-(1,2-dimethylpropyl)borane)は、2-メチル-2-ブテンをボラン(BH3)と反応させて得られるホウ素化試薬です。
名前の由来は Thx と同じく、置換基の慣用名 sec-iso-amyl 基から来ています。“アミル”は古い文献で使われていた名前で、いまの“ペンチル”にあたります。
ちなみに、“sec” は官能基がついている炭素が 2 級(secondary)であることを示します。
アルケンの種類によって、ぴったりのホウ素試薬は変わります。“反応条件を選ぶ”のも有機化学のセンス。いろんな試薬を触って、相性を見極めてみようね。
(3-4) キラルホウ素試薬で立体選択的付加(Ipc₂BH)
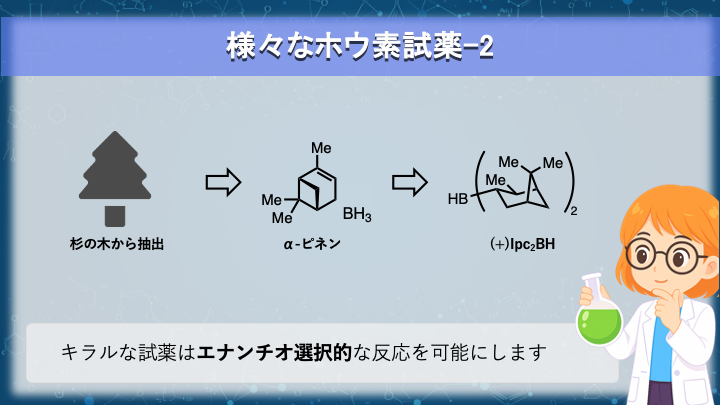
ボラン(BH3)は平面構造の分子で、上面と下面に立体的な違いがありません。でも──もし、そのホウ素にキラルなアルキル基をつけてみたら?
ここまでエナンチオ選択性には触れてきませんでしたが、キラルな試薬を使うと、生成物の立体中心に「どちらの鏡像体が多くできるか」という差が生まれます。この性質を活かした代表的な試薬が、ジイソピノカンフェイルボラン(Ipc2BH)。
(–)体と(+)体の二つの異性体がそれぞれ存在し、松の主成分 α-ピネンとボランの反応で調製されます。キラルな試薬は高価になりがちですが、天然から多く取れるキラルを原料にすれば費用も節約できますね!
Ipc2BH は嵩高い分、反応性はやや穏やかですが、その分だけ立体選択性が鋭く、多置換アルケンのヒドロホウ素化にも応用できます。さらに、より反応性の高いモノアルキルボラン IpcBH2 が使われることもあります。
エナンチオ選択性が生じる遷移状態を正確に描くのは少し難しいですが、#A ではその立体化学的モデルを詳しく扱う予定です。ここではまず、キラルなボランを使えば、キラルなアルコールを設計できる──その感覚を、少し感じてみてください。
🧭 まとめ
- ヒドロホウ素化酸化は、協奏的・syn 付加・アンチマルコフニコフ付加の三拍子。
- 立体障害が反応位置を左右し、置換基の少ない炭素にホウ素が導入される。
- 酸化段階では、HOO− の求核 → O–O結合切断 → σ結合移動 という電子の流れが本質。
- 試薬設計(9-BBN, ThxBH2, Sia2BH, Ipc2BH)で、位置・立体・選択性を自在に制御できる。
- 反応を“書く”のではなく、“理解して導ける”ようになることが本当のゴール。
🌸 最後に
今日も有機化学の勉強お疲れ様でした( ̄▽ ̄)b☆
国家試験でも、大学院入試でも頻出するのに、みんな暗記で済ませがちな範囲だったから、私もつい熱が入っちゃいました (≧▽≦)
疲れたら団子でも食べて休んでくださいね🍡
次回は「アルケンの反応⑤:付加環化反応」を取り扱います!
一気に C–C 結合を二つも作れる!そんな効率的な反応がアルダなんて!
……びっくりですよね (〃 ̄ω ̄〃ゞ💦
あなたにとって有機化学が少しでも笑えるものになりますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック









コメントを残す コメントをキャンセル