🧪 #U3 アルケンの反応②:協奏する分子たち
(ブルース有機化学 第7版/邦訳第5版 p176–230 準拠)
🌸 導入
研究に限らず、現代社会は比較と競争に満ちあふれています。疲れちゃう時もありますよね。そんな時は、静かに音楽を聴くのもいいリフレッシュになるのではないでしょうか。
実は化学の世界にも、“コンサート”🎶があるんです。複数の位置で同時に電子が動く反応、それを協奏反応(concerted reaction)といいます。語源は英語の “concert”=協奏。音楽でも楽器それぞれのリズムとタイミングが大事。化学でも、電子たちがぴったり息を合わせる瞬間があるんです。
この単語、とっても重要です。よく対になる概念として「段階的反応(stepwise reaction)」があります。二つを並べて覚えると、反応機構の理解がぐっと深まりますよ。
語源と感動とセットでインプットできた君。もう、この記事で伝えたいことの半分は終わりました。ありがとう。
……でも、「もうちょっと具体例が欲しい!」という君のために、アルケンの協奏反応――エポキシ化反応・ハロゲン付加反応・水素添加反応――を一緒に見ていきましょう。
それでは、始めましょ!
① エポキシ化反応 ― Prilezhaev(プリージャエフ)酸化っていうらしいー
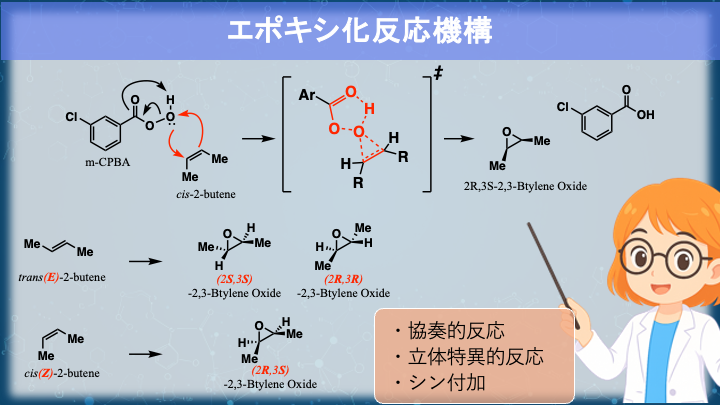
一言で説明すると、「アルケンに過酸をシン付加させて3員環エーテル(エポキシド)を作る反応」です。
まず、一つ覚えておいてほしいのは、ヘテロ原子同士の結合は切れやすいということ。ざっくり言えば、O–O や N–N のような結合は電子雲が狭い範囲に密集しすぎていて、電子どうしが反発しやすい。一方、Br–Br のような重原子結合では電子雲が広く分布していて、軌道の重なりが小さいためσ結合が弱くなります。このように、ヘテロ原子同士の結合は「切れやすい」結合なんです。
さて、エポキシ化では過酸(例:mCPBA)を用います。アルケンのπ電子が過酸のO–O結合を切るように、安息香酸側ではない酸素原子を攻撃します。この過程は一段階で完結し、カルボカチオンを経由しません。つまり、協奏的に電子が動く反応です。
生成物は酸素–炭素–炭素の三員環構造、エポキシド(オキシラン)。アルケンの同じ側に新しい結合ができるため、生成物はシン付加になります。
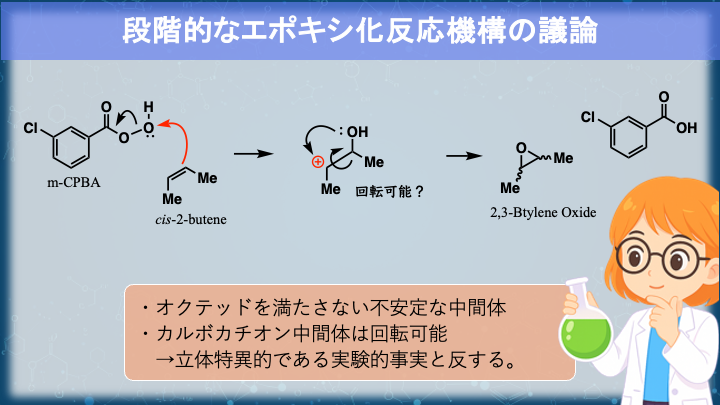
協奏反応である理由を理解するためには、段階的経路と比較してみるのが早いです。もし途中にカルボカチオンを経由するなら、一瞬とはいえ電荷分離が起き、反応の活性化自由エネルギーは高くなってしまいます。しかし協奏的に進むと、電荷の発生を最小限に抑えられるため、結果的により進みやすい。
実験的にも、アルケンの置換基配置がエポキシドにそのまま反映される「立体特異的反応」であることが確かめられています。つまり、途中に回転可能なカルボカチオンは存在していない。それが協奏反応である、確かな証拠です。
より直感的にまとめるなら、「アルケンとヘテロ原子(孤立電子を持つσ*求電子剤)との反応では、協奏的に3員環を構築する」と理解しておけばOKです。
② ハロゲンとの反応 ― ハロニウムカチオンって何?
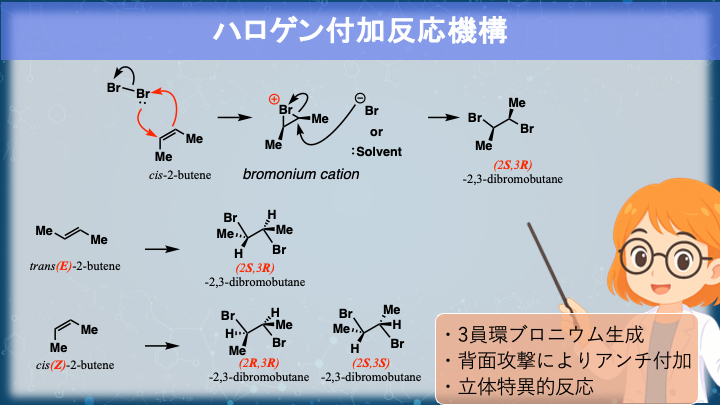
この反応を一言で説明すると、「アルケンにハロゲンを反応させると、ハロゲン原子と溶媒またはハロゲンイオンがアンチ付加したハロゲン化アルキルが得られる」というものです。
ハロゲンとの反応も、コツはエポキシ化と似ています。ハロゲン分子がアルケンに近づくと分極し、片方の原子がδ⁺となってπ電子の攻撃を受けます。その結果、3員環構造のハロニウムカチオンが生成します。この3員環型のカチオンは、オクテットを満たしている分、カルボカチオンよりも安定に存在できます。
とはいえカチオンなので、強い求電子性をもっており、溶媒やハロゲンイオンなどの求核剤が反応を続けます。攻撃は三員環の反対側から起こるため、生成物はアンチ付加になります。
つまり、ハロゲン付加反応の第1段階――ハロニウムイオンの生成――が、“電子の動きが同時に起こる協奏的反応”なんです。そしてこの中間体こそが、立体選択性を決める要の存在なんですね。
③ 水素添加反応 ― トランス脂肪酸を添えてー
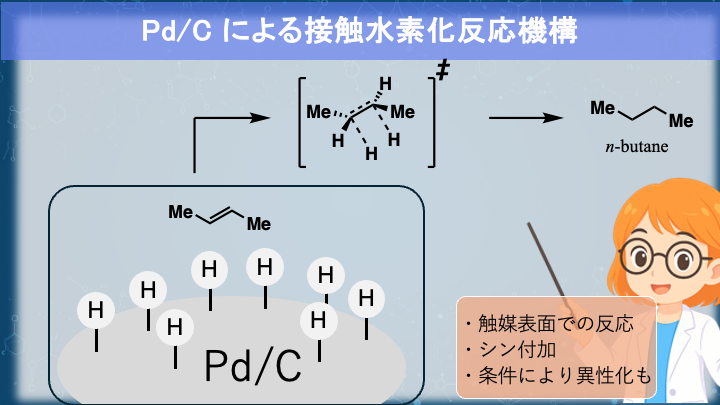
最後に、アルケンの水素添加(接触還元)を見てみましょう。この反応は、「パラジウム炭素がアルケンと水素ガスを活性化させて、シン付加でアルカンを得る反応」です。
パラジウム(Pd/C)やニッケル(Ni)などの金属触媒表面で、水素分子(H₂)が結合を切られて原子状の水素として吸着されます。そこにアルケンが近づき、π電子が金属表面に引き寄せられながら、同時にHが両炭素に付加します。
この反応も電子の動きと結合形成が協奏的に起こる、典型的なシン付加です。ただし、条件によってはアルケンの異性化が起こることがあります。つまり、シス型がトランス型に変わってしまう。アルケンが自由に回転できる条件では、嵩高い置換基が離れるE体の方が熱力学的に安定になるためです。
#U2で扱った「バターとマーガリン」の話、あの現象の正体がまさにこれです。マーガリン製造では、液状の植物油を部分的に還元して固形化しますが、その過程でシス脂肪酸の一部が異性化して、トランス脂肪酸が生じてしまうのです。
🔬 博士aIRaの余談:
実際に触媒還元を行うと、条件によっては還元が完全に進まず、アルケンの異性化が起こることもあります。化学者たちは、溶媒や触媒(金属の種類や担体)を工夫しながら、反応条件をチューニングしているんですね。
🧭 まとめ
- ヘテロ原子同士の結合は切れやすく、反応を動かす“きっかけ”になる。
- ヘテロ原子のσ*求電子剤とアルケンの反応は3員環を形成する。
- 協奏反応では、電子が同時に動き、立体化学的にも制御された生成物が得られる。
- 水素化は条件によってアルケンの異性化を伴い、トランス脂肪酸生成の要因にもなる。
🌸 最後に
今日の“協奏”の授業が皆さんのリフレッシュになれば、指揮者の私も嬉しい限りです。
次回のテーマは有名な「マルコ」についてです。そう、不死鳥になれる海賊団の隊長でも、進撃しそうなキャラでもなく、有機化学界の“マルコ”──Markovnikov(マルコフニコフ)先生の経験則!
カルボカチオンの安定性から、求電子付加の位置選択性、転位反応まで。博士aIRaがじっくり語ります。
(著名な先生に対して無礼でした。お詫びします。)
高校生でも知っている、有名な名前。まだ知らない人!流行に乗り遅れてるので必見です!
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
🫧 #Cでは aIRa の日常を気ままに発信中!
研究の裏側やカフェ巡り、香水、ちょっとしたつぶやきまで。
▶ Conversation et Café − aIRaの日常 −
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック




コメント