- 末端アルキンがなぜ安定なのかを混成軌道のs性を元に説明できる
- アセチリドイオンをどう使うのかを説明できる
- これまでのアルキンアルケンの知識を応用して逆合成解析にチャレンジする
- アルケン、アルキンの求電子付加反応
- 酸性度塩基性度の比較
- 混成軌道についての基礎知識
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に
「理解でつなぐ大学有機化学」をかわいくお届けします。
「末端アルキンは酸性である」ということは、高校までの化学の常識をくつがえす、衝撃を感じた記憶があります。
高校化学で扱う酸は、塩酸や酢酸のように水溶液中で明確に酸性を示す物質でした。
しかし有機化学では、酸とは「プロトンを与えることができる化学種」(ブレンステッド酸)を指します。
末端アルキンは液性としてはほぼ中性ですが、有機化学ではこの性質が重要な反応設計の出発点になります。
この記事では、
- なぜ末端アルキンが酸として振る舞うのか
- その性質が合成化学でどのように利用されるのか
を順を追って整理していきます。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
文字が苦手な人も図を追えるように構成しているので、参考書のつもりでゆっくりどうぞ。
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
今日解説するポイントを確認

今日解説するポイントをまず提示します。
今日の講義は、末端アルキンの酸性度を他の炭化水素と並べて差を見るところから始めます。
この講義は大きく二部構成です。
前半:なぜ末端アルキンの酸性度は“相対的に”高いのか
そのために、次の3点を順に押さえます。
- 末端アルキンが脱プロトン化して生じるアニオンを アセチリドイオン と呼ぶ
- 酸性度の差は、結合している炭素の 混成軌道(sp/sp²/sp³) の差として表れる
- 混成軌道の s性 は「電子が核の近くに居られる度合い」としてアニオン安定性に効く
後半:この“少し高い酸性度”が合成で何を可能にするのか
末端アルキンの酸性度が意味するのは、結局のところ
「簡便な操作で炭素アニオン(=アセチリド)を求核剤として活用できる」
という一点です。
そこから合成上の利点が2つに分岐します。
- 炭素求核剤として C–C結合形成 に使える
- 生成物のアルキンを 官能基変換の足がかり として残せる
まずは「sp炭素アニオンがなぜ安定か」を説明できればノルマ達成!
末端アルキンの酸性度が高い理由=アセチリドの安定性
強塩基で末端アルキンが脱プロトン化される
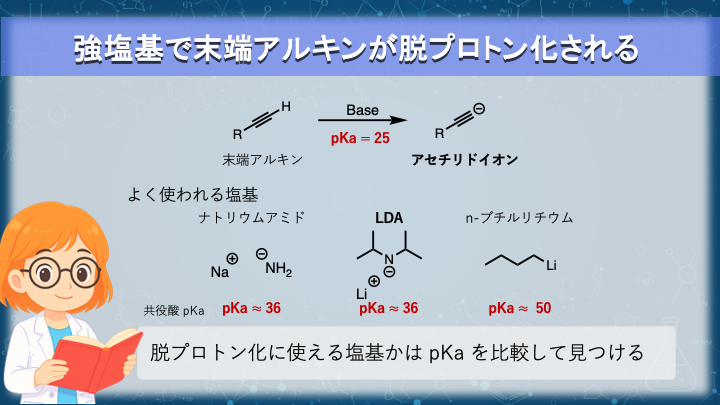
末端アルキンに強塩基を加えると、炭素上のプロトンが引き抜かれます。
こうして生じる炭素アニオンを“アセチリドイオン”と呼びます。
ここで一つ重要な点があります。
末端アルキンのpKaは およそ25 とされており、アルコール(pKa ≈ 16)や水(pKa ≈ 15)よりもかなり弱い酸です。
そのため、一般的な塩基では脱プロトン化はほとんど進みません。
実際の合成では、より強い塩基を用いてこの平衡をアセチリド側に押し出します。
よく使われる塩基として次のものがあります。
① ナトリウムアミド (NaNH₂) :共役酸 NH₃ pKa ≈ 36
② リチウムジイソプロピルアミド (LDA):共役酸 pKa ≈ 36
③ n-ブチルリチウム (n-BuLi):共役酸 pKa ≈ 50
これらの強塩基を用いることで、末端アルキンから安定な炭素アニオンであるアセチリドイオンを発生させることができます。
pKa集として“Evans先生がまとめたpKa集”も活用するといいと思います。
混成軌道(sp/sp2/sp3)で酸性度が異なる
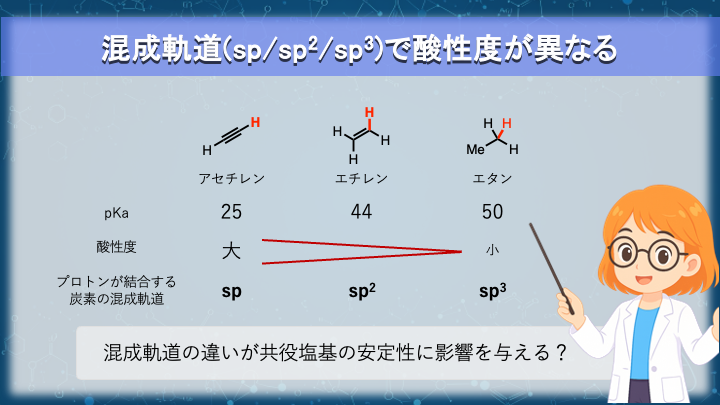
前節では、末端アルキンが強塩基によって脱プロトン化されることを確認しました。
しかしここで、多くの人が違和感を覚えるかもしれません。
「末端アルキンは酸性度が高い」と言われても、pKaが25もある物質を酸と呼ぶのは少し奇妙に感じます。
ここで重要なのは相対的な比較です。
炭化水素のC–H結合の酸性度を並べてみると次のようになります。
エタン pKa ≈ 50
エチレン pKa ≈ 44
アセチレン pKa ≈ 25
どれも強い酸ではありません。
しかしこの三つの間には、大きな差が存在しています。
この違いを生み出しているのが、C–H結合を持つ炭素の混成軌道です。
エタンでは sp³
エチレンでは sp²
アセチレンでは sp
というように、結合している炭素の軌道が異なります。
pKaの比較から、sp³炭素と結合したプロトンよりもsp炭素と結合したプロトンの方が脱プロトン化しやすいことが分かります。
言い換えると、生成するアニオンの安定性に違いがあるということです。
では、なぜsp炭素上のアニオンは安定なのでしょうか。
その理由を次節で見ていきます。
s性が高いと電気陰性度が高くなる理由(軌道の形から)
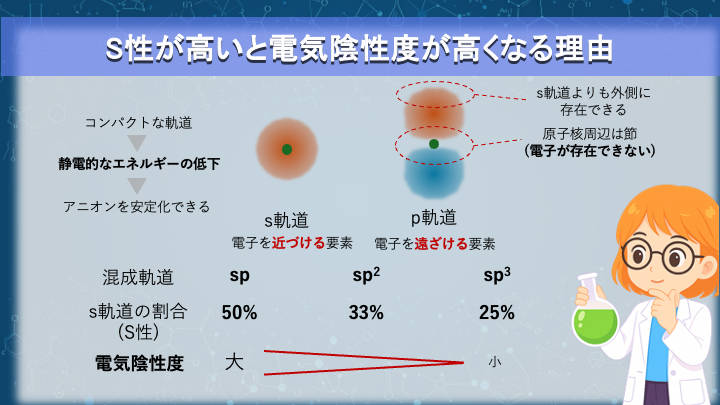
混成軌道の中にs軌道がどれくらい含まれているかをs性と呼びます。
sp³、sp²、sp混成軌道では、この割合が次のように変化します。
sp³ :25% s性
sp² :33% s性
sp :50% s性
つまり、sp炭素では最もs軌道の割合が大きくなっています。
ここで、s軌道とp軌道の形を見てみましょう。
s軌道は原子核の周囲にコンパクトに分布する球状の軌道です。
一方、p軌道は原子核を中心に節を持ち、電子はより外側の領域に分布します。
この違いのため、s軌道の割合が大きいほど電子は原子核により近い位置に存在することになります。
負電荷を持つ電子が原子核(正電荷)に近づくほど、静電的な引力によってエネルギーは低下します。
その結果、sp炭素上のアニオンは他の炭素アニオンよりも安定になります。
この「電子を強く引きつける性質」を、化学では電気陰性度が高いと表現します。
つまり
s性が高い炭素ほど電子を引きつけやすく、アニオンを安定化できるということです。
sp炭素アニオンが安定になる理由まとめ
ここまでで、第2章の内容を整理しておきましょう。
末端アルキンのC–H結合は、他の炭化水素と比較して酸性度が高く、アミドアニオンなどの強塩基によって脱プロトン化することができます。
このとき生成する共役塩基がアセチリドイオンです。
炭素アニオンの安定性は、炭素の混成軌道に含まれるs性によって大きく変化します。
sp³ < sp² < sp
の順にs性が大きくなり、s性が高いほど電子は原子核の近くに存在できるため、負電荷は安定化します。
その結果、sp炭素上に負電荷を持つアセチリドイオンは比較的安定な炭素アニオンになります。
ここまでで、末端アルキンからアセチリドイオンを安定に発生させられる理由が見えてきました。
次は、このアセチリドイオンが有機合成でどのように使われるのかを見ていきます。
アセチリドイオンで何ができるのか
アセチリドイオンは強力な炭素求核剤である
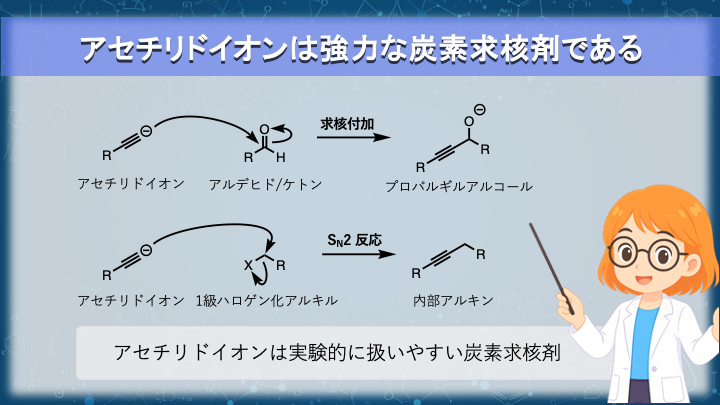
アセチリドイオンは比較的安定な炭素アニオンでありながら、求核剤として高い反応性を持っています。
アセチリドイオンは炭素上に完全な負電荷を持つため、電子密度が高く、求電子性のある分子と容易に反応します。
これまでの学習では、アルケンが求核剤として働く反応を見てきました。
しかしアルケンの場合、求核性の源はπ電子であり、分子全体としては中性です。
そのためアルケンは、プロトンやホウ素化合物のような強い求電子剤とは反応しますが、ハロゲン化アルキルやカルボニル化合物のような求電子剤とは通常の条件では反応しません。
一方で、アセチリドイオンは炭素上に負電荷を持つため、これらの求電子剤とも反応することができます。
特に重要なのは、炭素–炭素結合を形成できる点です。
アセチリドイオンは比較的安定な炭素アニオンであるため取り扱いやすく、求電子剤と反応させることで新しいC–C結合を形成することができます。
この性質により、アセチリドイオンは有機合成における強力な炭素求核剤として利用されています。
+ と – がくっつく有機化学において、どんな求核剤、求電子剤を組み合わせられるかがとても重要です。
ハロゲン化アルキルによるSN2でアルキル化
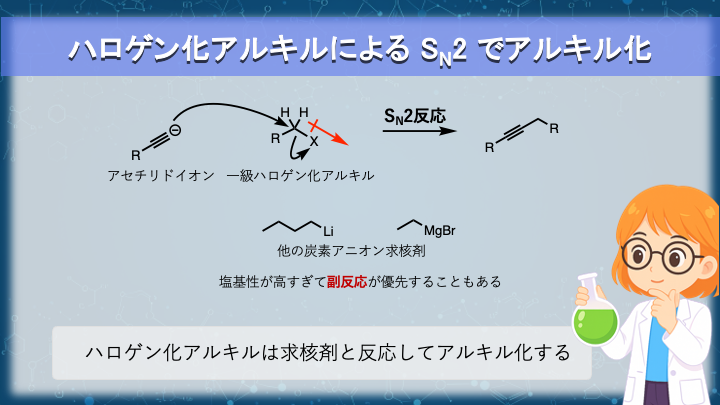
アセチリドイオンを求核剤として利用すると、ハロゲン化アルキルと反応して新しい炭素–炭素結合を作ることができます。
ハロゲン化アルキルでは、炭素とハロゲンの結合が分極しており、炭素は部分的に正電荷を帯びています。
そのため、求核剤がこの炭素に攻撃すると、脱離基であるハロゲンが同時に離脱し、新しい結合が形成されます。
この反応を SN2反応(求核置換反応) と呼びます。
アセチリドイオンは炭素上に負電荷を持つ強い求核剤であるため、ハロゲン化アルキルに対してSN2反応を起こしやすい特徴があります。
この反応により、アセチリドイオンの炭素にアルキル基が導入され、炭素–炭素結合を効率よく形成することができます。
炭素アニオン求核剤の多くは反応性が高すぎて扱いにくい場合がありますが、アセチリドイオンは比較的安定であり、合成設計の中で扱いやすい炭素求核剤の一つです。
このため、アセチリドイオンを用いたSN2反応は有機合成において、炭素骨格を伸ばす基本的な手法として利用されています。
アルキンを官能基相互変換させて多様な炭化水素を構築
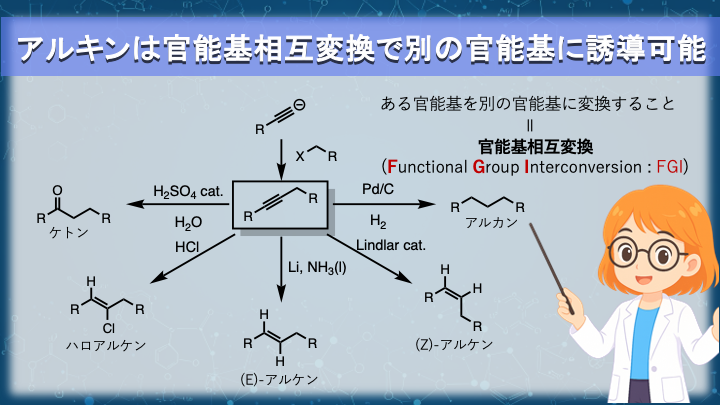
アセチリドイオンを利用する利点は、炭素–炭素結合を形成できることだけではありません。
もう一つ重要なのは、生成物として得られるアルキンが多様な官能基へ変換できる点です。
これまでの学習でも見てきたように、アルキンはさまざまな反応条件で官能基を変化させます。
例えば
Pd/Cによる水素化還元 → アルカン
酸性条件での水和反応 → ケトン
ハロゲン付加 → ジハロ化合物
といったように、アルキンは多くの官能基へ変換することができます。
このように、ある官能基を別の官能基へ変換する操作を
官能基相互変換(Functional Group Interconversion : FGI)
と呼びます。
アルキンはこのFGIの選択肢が豊富な官能基であり、合成の途中に導入しておくと、その後の反応設計の自由度が大きく広がります。
つまり、アセチリドイオンを用いたC–C結合形成は単に炭素骨格を作るだけでなく、その後の官能基変換を見据えた合成設計の出発点にもなるのです。
アセチリドイオンは炭素同士を繋ぐ出発点になる
ここまでで、アセチリドイオンを利用すると
- C–C結合を形成できること
- アルキンを官能基変換の起点として残せること
を見てきました。
これらの特徴は、逆合成解析を行うときに特に威力を発揮します。
逆合成解析とは、目的の分子から出発して、より単純な分子へと段階的に分解しながら合成経路を設計する考え方です。
ここでは実際に、アセチリドイオンを利用した合成ルートを考えてみましょう。
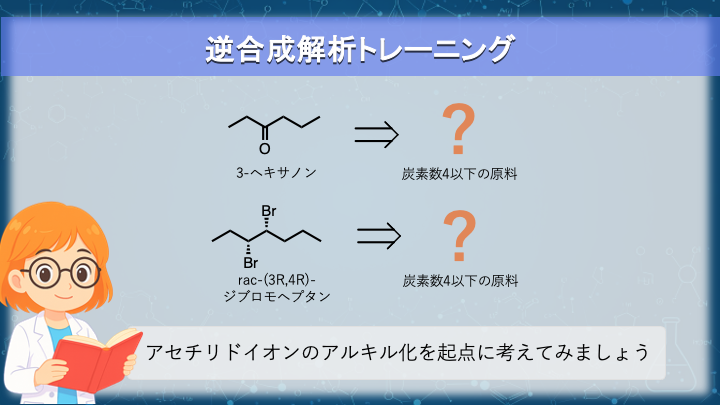
次の二つの分子について、4炭素以下の原料になるまで逆合成解析してみてください。
答えがこの下に表示されます。ぜひサラッと一度解いてみてから閲覧してください
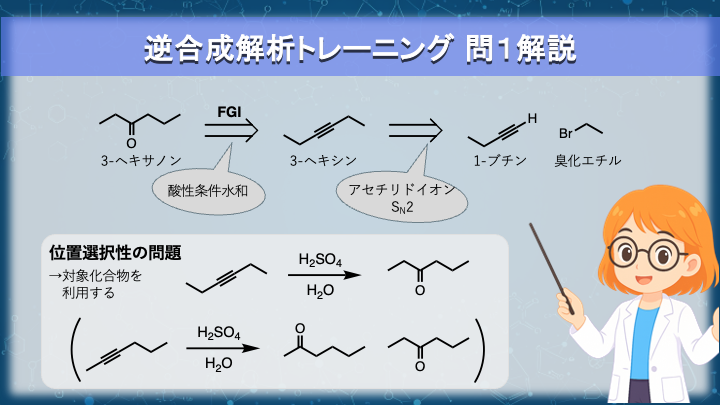
ターゲットは 3-ヘキサノン です。
ケトンはアルキンの水和反応を経て生成できるため、まずアルキンへと官能基相互変換 FGI します。
候補として
- 2-ヘキシン
- 3-ヘキシン
が考えられます。
3-ヘキサノンでは両側が対称なため、水和の位置選択性を考える必要がありません。
そのため 3-ヘキシン を選ぶと合理的です。
次に、このアルキンをC–C結合の位置で切断します。
すると
- 1-ブチン
- 臭化エチル
に分解できます。
すなわち、アセチリドイオン + ハロゲン化アルキルのSN2反応によって、この炭素骨格を構築できることがわかります。
ケトエノール互変異性化は#U11で取り扱いました。
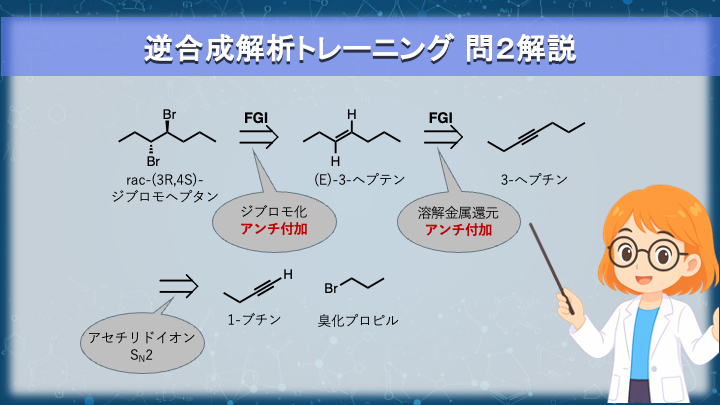
ターゲットは rac-(3R,4S)-3,4-ジブロモヘプタン です。
vic-ジブロモアルカンは、アルケンの臭素付加(アンチ付加)によって合成できます。
したがってまずアルケンへ官能基相互変換 FGI します。
アンチ付加を考慮すると、出発物質は E-3-ヘプテン が適切です。
次に、このアルケンをどのように合成するかを考えます。
E体アルケンは、アルキンの溶解金属還元(Na/NH₃など)によって得ることができます。
そこでさらに逆合成すると3-ヘプチン にたどり着きます。
このアルキンをC–C結合で切断すると
- 1-ブチン
- 1-ブロモプロパン
という4炭素以下の原料に分解できます。
ここでも、アセチリドイオンによるSN2反応を用いることで炭素骨格を構築できることがわかります。
アルケンのジブロモ化は#U3、溶解金属還元は#U12で解説しています!思い出せなかった人はぜひ復習してください。
まとめ
末端アルキンの酸性度は、単なる性質の説明にとどまりません。
それは炭素–炭素結合形成の出発点になる性質です。
今回の内容を整理すると次の二点になります。
- 末端アルキンが脱プロトン化して生じるアニオンをアセチリドイオンという
- 炭素の混成軌道では、s軌道の割合(s性)が大きいほど電子を原子核の近くに保持できる
- そのため、sp炭素上のアニオンは比較的安定になる
- このアセチリドアニオンはSN2反応などによってC–C結合形成に利用できる
- さらにアルキンは多くの官能基へ変換できるため、官能基相互変換(FGI)の出発点としても有用である
① なぜ末端アルキンは酸性なのか
② その酸性度がなぜ重要なのか
今回は逆合成解析の考え方にも少し触れてみました。
有機合成では、このように分子をより単純な構造へ分解しながら合成経路を設計していきます。
最後に
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
今回でブルース有機化学の7章の範囲を完了いたしました!
最近、中の人が忙しくて、更新頻度が若干落ちてしまいました。
反省反省。。
3月中には8章の内容を終わらせるのが目標なので、今月あと二つは執筆する予定です。
講義シリーズのサムネイルは、一応講義の内容からインスピレーションを受けて作成しているのですが、#U10のサムネイルでギターを採用するに至った理由を想像できる人は何人現れるのでしょうか笑
当たり前ですけど、顔がドアップで見やすいサムネイルって、クリック率が高いというのが最近の知見です。
講義記事だと分からなくても、なんかクリックしたくなる、そんなサムネイルを研究したいものです。
次回は、8章 「共鳴」 に進みます。
人と話すときにうまく話を回すくせに、家庭では静かであるというお父さんとの共通点を見つけたときに、お父さんとの共鳴を感じて複雑な気持ちになります。
私という存在は、お父さんとお母さんの共鳴混成体である。
というのが、共鳴のイメージなのですが、これを理解するために生物の知識がそこそこ必要になってくるので、
たった今、この比喩は棄却しました。
次回をお楽しみに!
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック





コメントを残す コメントをキャンセル