- Pd/C による接触還元でアルカンが得られる理由を説明できる
- Lindlar 触媒の触媒設計を説明できる
- 溶解金属還元でなぜtrans体が優先するのか説明できる
- アルケン、アルキンの求電子付加反応
- 反応機構を書くための基礎知識
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に
「理解でつなぐ大学有機化学」をかわいくお届けします。
アルキンの還元反応を学ぶとき、「Pd/Cならアルカン、Lindlar触媒ならcis、Birch還元ならtrans」と覚えた経験はありませんか。
この対応は便利で早く、効率的にみえます。
でも「なぜそうなるのか」と聞かれると、説明が止まってしまいます。
立体選択性は結果です。
実は、その結果が生まれた“途中の情景”を思い浮かべられるかどうかで、暗記は導出に変わるのです。
三角関数の和積の公式は暗記するんじゃなくて、導出すればいいとは言いますが、有機化学でも同じように暗記を減らせるとしたら嬉しいですよね?
今回は、アルキンの還元を通して、cis/trans 立体がどの段階で決まるのかを見直していきます。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
文字が苦手な人も図を追えるように構成しているので、
参考書のつもりでゆっくりどうぞ。
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
アルキン還元におけるシン付加・アンチ付加の整理ポイント
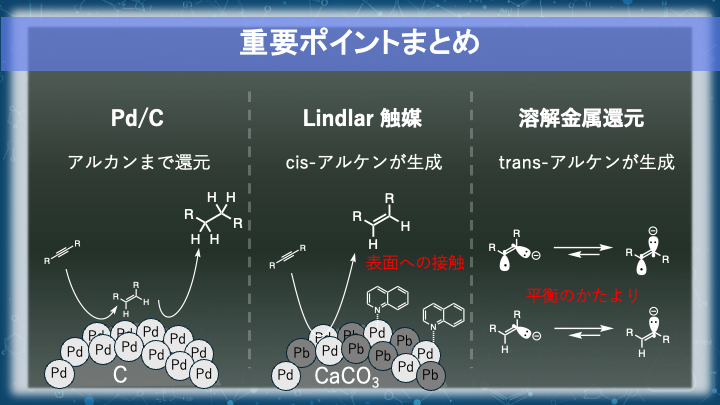
今回扱うのは、アルキンの還元を行う三つの手法です。
重要なのは「何ができるか」ではなく、立体がどの段階で決まるのかを見ることです。
一つ目は Pd/C による接触水素化です。
金属表面で連続的に水素が供給され、アルキンはアルケンを経てアルカンまで還元されます。
立体は“表面付加の段階”で方向づけられます。
二つ目は Lindlar 触媒です。
反応は同じく金属表面で起こります。
しかし触媒が弱められているため、アルケンの段階で反応が停止します。
ここでも立体は“表面付加(シン付加)”で決まります。
三つ目は溶解金属還元 (Birch還元) です。
反応は溶液中で一電子還元から始まります。
ラジカルアニオン、ビニルアニオン中間体を経由し、その段階の”平衡の位置”で付加の向きが決まります。
この三つを、
「どの段階で立体が確定したか」という視点で比較します。
全て読み終わった後ここに戻ってくると、より深くポイントを刻むことができます。
アルキンの接触還元(Pd/C)とシン付加
Pd/Cによる接触還元はなぜシン付加になるのか
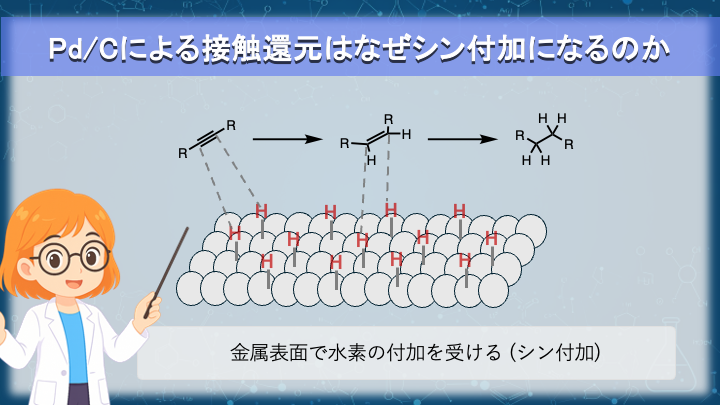
Pd/C とは炭素粉末に0価のパラジウムを吸着させた不均一触媒で、水素雰囲気下でアルケンやアルキンを還元することができます。
専門用語で「接触還元」「接触水素化」「水素添加」と呼ばれます。
接触という名前から想像できると思いますが、この反応のポイントは金属表面上で全ての一連の流れが起こる点です。
水素分子はまず表面に吸着し、Pd 原子との相互作用により活性化されます。
その金属表面に対してアルキンが接近していくことで水素化されます。
アルキンに対して、活性化された水素に上下で挟み込まれることはなく、同じ側から導入 (シン付加) されるのです。
アルキンが還元を受けるとアルケンになります。
Pd/Cを用いる条件では、反応はアルケンで停止せずにアルカンまで還元されてしまいます。
#U3ではアルケンがPd/Cによって還元されることを学びました。
接触還元ではアルキンとアルケンで反応性がどう違うか
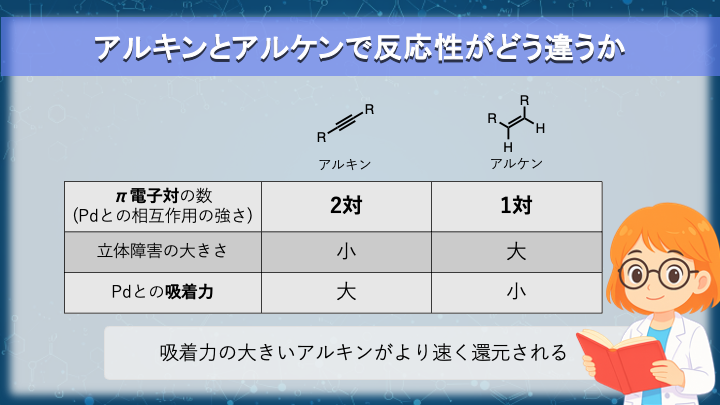
アルキンの反応では、過剰反応の有無、すなわち生成物のアルケンとの反応速度の差を比較する必要があります。
接触水素化において、アルキンとアルケンの反応性の差をもたらすのはどんな要因なのでしょうか。
金属表面での水素化では、基質がどれだけ強く金属と相互作用できるかが重要になります。
相互作用の中心は π 電子です。
アルキンは二本の π 結合を持ち、電子密度が高く、金属表面と強く相互作用しやすい構造です。
一方、アルケンは π 結合が一本であり、生成後は置換基も増えるため、表面への接近や吸着がやや不利になります。
したがって一般に、金属表面での水素化速度は アルキン > アルケン と考えられます。
しかし「速い」ということと「そこで止まる」ということは同義ではありません。
アルケンも依然として表面に吸着し、水素化されうる基質です。
速度差があるにもかかわらず、なぜ停止が難しいのでしょうか。
次で見ていきます。
接触還元でアルケンがさらに還元される理由
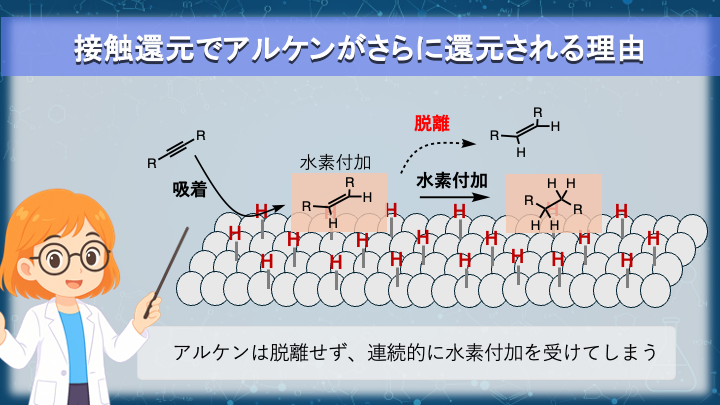
アルケンで停止させることが難しい理由は、反応が金属表面上で連続的に進行する構造にあります。
アルキンが還元されてアルケンになると、そのアルケンはすぐに溶液中へ拡散するとは限りません。
金属表面に吸着した状態のまま、次の水素付加を受ける可能性があります。
つまり、
アルキン → アルケン → アルカン
という段階が、同一の吸着状態の延長線上で進行します。
アルケンが「反応できない基質」にならない限り、連続的水素化は避けにくいのです。
Lindlar触媒によるアルキンの部分還元(cis-アルケン生成)
Lindlar触媒の組成と被毒化の意味
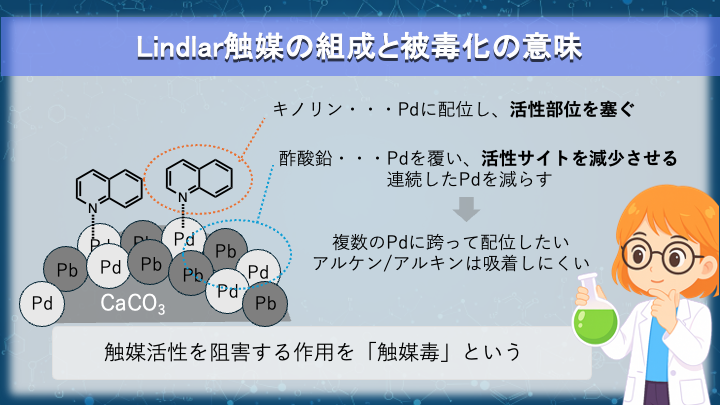
Lindlar 触媒は、部分還元を可能にするために設計された Pd 触媒です。
基材には炭酸カルシウム上に分散した Pd が用いられ、これに酢酸鉛で処理し、さらにキノリンを添加して使用します。
酢酸鉛は Pd 表面の一部を鉛原子で覆い、Pd 原子が連続して並ぶ「活性サイト」を減少させます。
アルキンやアルケンは、複数の Pd 原子にまたがる形で吸着します。
連続した Pd サイトが減少すると、吸着の安定性は低下します。
キノリンは Pd に配位し、表面の活性部位をさらに減少させます。
このように触媒活性を意図的に抑制する作用を「触媒毒」と呼びます。
邪魔の多いPd触媒というイメージを持ちましょう。
なぜLindlar触媒ではアルケンが還元されないのか
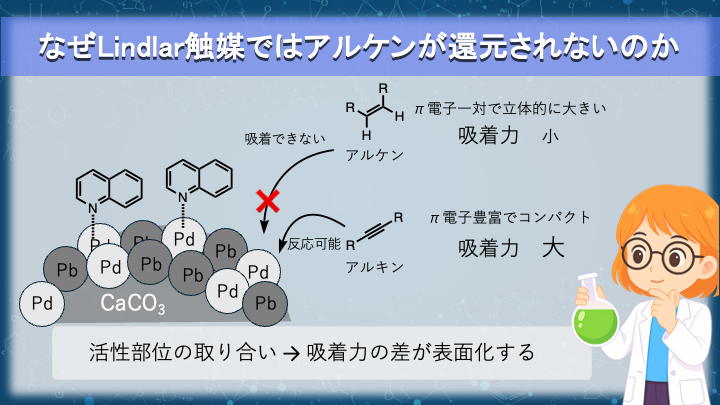
Lindlar 触媒では、Pd 表面の有効サイトが大きく制限されています。
この条件下では、基質同士が触媒表面で競合します。
アルキンは Pd との相互作用が強く、被毒化された触媒は表面でも十分に吸着することができます。
一方、アルケンは相対的に吸着力が弱く、被毒化された表面では安定に保持されにくくなります。
さらにキノリンが Pd に配位することで、表面の空きサイトは限られた状態になります。
その結果、アルキンは吸着・反応できるが、生成したアルケンは吸着競争において不利となり、表面から脱離しやすくなります。
このように、吸着強度の差と競合関係によって、アルケンのさらなる水素化が抑制されます。
Lindlar触媒でcis-アルケン (シン付加) が得られる理由
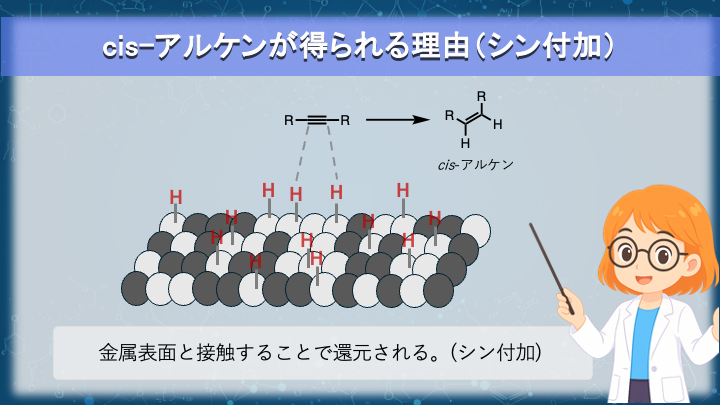
Lindlar 触媒においても、水素化の基本機構は Pd/C と同じです。
水素分子は金属表面で活性化され、基質は表面に吸着した状態で水素を受け取ります。
アルキンは金属表面に平行に吸着し、その π 系が表面と相互作用します。
この状態では両炭素は同じ面を金属に向けています。
活性化された水素原子は、金属表面から基質へと供与されます。
そのため、水素は同じ側から同時に導入されます。
金属の反対側から水素が攻撃する経路は存在しません。
このため付加様式は必然的にシン付加になります。
アルキンに対するシン付加は、結果として cis(Z)-アルケンを与えます。
接触還元とLindlar触媒に共通する「シン付加」の考え方
ここまでの内容を整理します。
Pd/C による接触水素化も、Lindlar 触媒による部分還元も、いずれも金属表面上で進行する水素化反応です。
水素分子は金属表面で活性化され、基質は吸着した状態で水素を受け取ります。
この「表面吸着状態」において、水素は常に同じ面から供与されます。
したがって、付加様式は共通してシン付加です。
両者の違いは立体ではなく、「どこで反応が停止するか」にあります。
Pd/C ではアルキンもアルケンも吸着しやすく、連続的に水素化が進行します。
一方、Lindlar 触媒では活性サイトが制限され、吸着力の強いアルキンのみが十分に反応できます。
立体は金属表面で決まり、選択性は吸着の強弱で決まる。
アルキンの溶解金属還元(Birch還元)とアンチ付加
溶解金属還元(Birch還元)の基本的な反応像
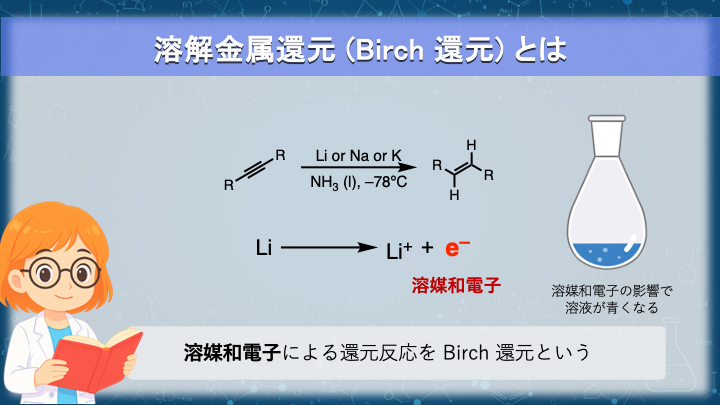
溶解金属還元 (Birch 還元) は、
アルカリ金属を液体アンモニア中で用いる還元法です。
これまでに解説した接触還元とは性質が大きく異なります。
金属表面での水素付加ではなく、溶液中で電子が直接移動する反応です。
金属を液体アンモニアに加えると、価電子が放出され、溶液は特徴的な青色を示します。
その様子がわかりやすいYoutube動画を共有しておきます。
放出された電子はアンモニア分子によって囲まれ、溶媒中で安定化されます。
この電子を「溶媒和電子」と呼びます。
溶媒和電子は強力な還元剤であり、この反応は一電子移動から開始します。
低温条件 (約 −78 ℃) は液体アンモニアを保持し、生成するラジカル種やアニオン種を安定に扱うために必要です。
次節では、この一電子還元がどのような中間体を形成させるのかを確認します。
Birch還元は、アルキンの還元とベンゼン環の還元を両方指して言います。
どちらも液体アンモニアに溶解させた金属による一電子還元機構で進行します。
Birch 還元の反応機構の流れを確認
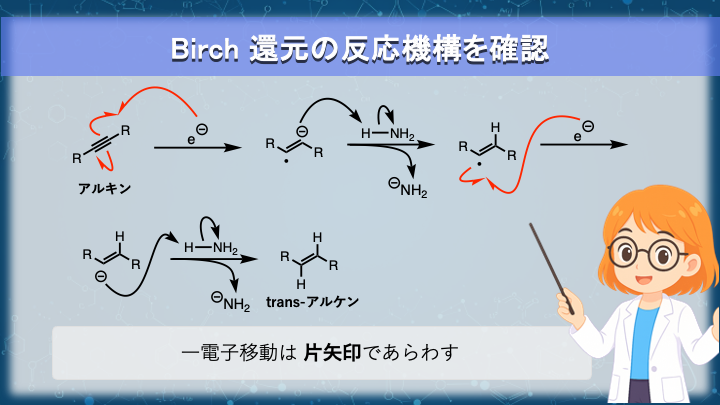
Birch 還元の反応機構を整理します。
まず、溶媒和電子がアルキンに一電子を供与します。
その結果、三重結合の π 系に電子が入り、ラジカルアニオンが生成します。
このラジカルアニオンは塩基性を持ち、溶媒であるアンモニアからプロトンを受け取ります。
これにより、ビニルラジカルが生成します。
続いて再び溶媒和電子が一電子を供与し、ビニルアニオンが生成します。
最後にこのアニオンがプロトン化され、アルケンが得られます。
この反応は、
「電子付加 → プロトン化 → 電子付加 → プロトン化」
という電子移動とプロトン移動が交互に進行する機構です。
一電子還元の曲がった矢印は片矢印になっていることに注意しましょう。
溶解金属還元でtrans体 (アンチ付加) が生じる理由①
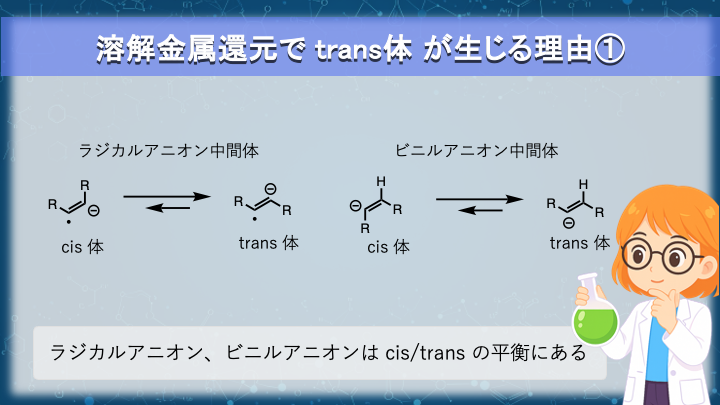
反応機構の流れを確認したので、次に立体がどの段階で決まるのかを考えます。
鍵となるのは、ラジカルアニオンおよびビニルアニオン中間体です。
これらの中間体では、三重結合の π 系に電子が加わることで結合次数が低下し、アルケンに近い構造 (平面構造) をとります。
この状態では、cis/ trans に相当する配置の間で実質的に平衡が成立します。
したがって、最終生成物の立体はこの平面中間体の段階に由来します。
溶解金属還元でtrans体が安定になる理由②
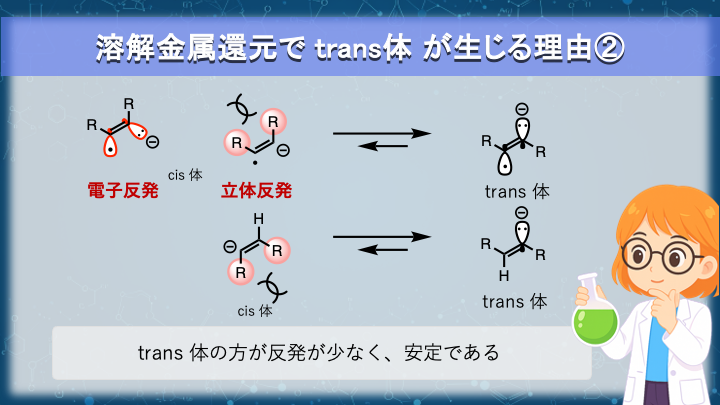
ラジカルアニオンおよびビニルアニオンは、cis/ trans に相当する配置の間で平衡にあります。
Birch還元反応で trans アルケンが優先して生成する理由は、この平衡が trans 側に偏っているからです。
平衡の偏りは次に示す二つの反発要因によって生じます。
まず一つ目は 立体反発 です。
アルキン由来の二つのアルキル置換基は、体積を持つ原子団です。
cis 配置ではそれらが空間的に近接し、電子雲同士が強く押し合うためエネルギーが上昇します。
trans 配置では原子団間の距離が離れ、この幾何学的な反発が小さくなります。
二つ目は 電子反発 です。
ラジカルアニオンでは、一方の炭素に不対電子 (ラジカル) が、もう一方に電子対 (アニオン) が存在します。
これらが同じ側 (cis) に位置すると、電子同士の静電的な反発が増大します。
このように、原子団のかさによる立体反発と、ラジカルとアニオンの電子反発の両方がtrans 型を安定化させます。
その安定化した配置でプロトン化が進行するため、最終生成物も trans-アルケンとなります。
Birch 条件でアルケンは還元を受けるのか
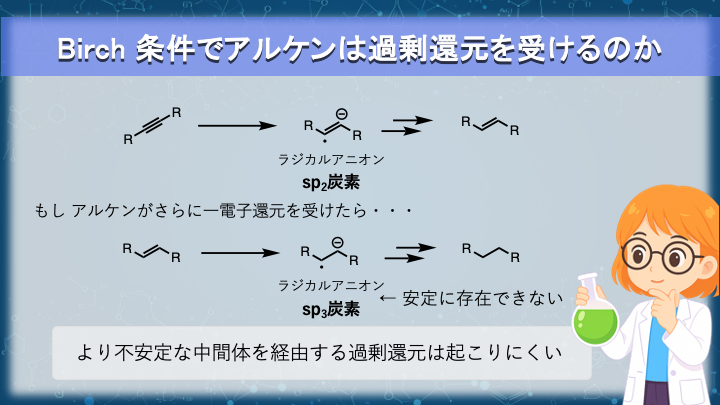
ここまで、溶解金属還元が一電子移動から進行し、ラジカルアニオンおよびビニルアニオンを経由することを確認してきました。
では、生成したアルケンは同様に還元を受けるのでしょうか。
紙面上では、アルケンも一電子還元を受けることは可能です。
しかし、実際の反応条件ではアルキンの還元が優先して進行し、生成したアルケンがさらに還元されることは通常起こりません。
その理由は、中間体の安定性の違いにあります。
アルキンが一電子を受け取って生じるラジカルアニオンでは、負電荷はビニル位(sp²炭素)に位置します。
一方、アルケンが同様に還元を受けると、より不安定なアルキル位(sp³炭素)に負電荷を持つ中間体を経由することになります。
一般に、sp²炭素上のアニオンはsp³炭素上のアニオンよりも安定であることが知られています。
この安定性差は、電子がより原子核に近い軌道に存在できることに由来します。
中間体の安定性が低いほど、その生成には大きなエネルギーが必要になります。
したがって、アルケンの一電子還元はアルキンよりも進行しにくく、結果として過剰還元は起こりにくいと考えられます。
この安定性差が、選択的にtrans-アルケンが得られる理由の一つとなっています。
まとめ:シン付加・アンチ付加を理由とセットで整理する
今回解説したアルキンの還元反応についてまとめます。
水素の付加様式とその理由、そして過剰還元の有無について整理します。
● Pd/CおよびLindlar触媒
→ 金属表面上で水素が同じ面から付加する
→ したがってシン付加で進行する
● Pd/C
→ 触媒表面に連続した活性部位が存在する
→ アルケンも吸着できるため過剰還元が起こりうる
● Lindlar触媒
→ 触媒毒により活性部位が制限される
→ アルケンは十分に吸着できず、還元は停止する
● Birch還元
→ 溶液中で一電子移動が起こる
→ 平面中間体を経由し、trans体が優先する
→ 選択性は立体反発と電子反発によって決まる
同じ「水素の付加」でも、
金属表面反応なのか、溶液中の一電子反応なのかで
立体の決定機構は本質的に異なります。
終わりに
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
Birch還元では、ラジカルアニオンやビニルアニオンといった、普段あまり見慣れない中間体が登場しました。
「シン付加」「アンチ付加」と暗記するだけでなく、その背後にある反応場や中間体の安定性に目を向けられたなら、今回の学習は十分意味があるのかなと思います。
有機化学は、結果だけを見る学問ではありません。
途中で何が起こっているのかを想像する力が、理解を一段深くすると私は考えます。
今回で、アルキンを自在に還元する手法を学びました。
次回は、アルキンの最後の反応、アセチリドイオンの化学へ進みます。
“安定な炭素アニオン”とは何か。
なぜ安定な炭素アニオンが重要なのか。
私が有機化学を好きになれたきっかけである”逆合成解析”についても説明します。
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック





コメント