- 共鳴寄与体を羅列し、安定性について議論できる
- 電子が非局在化するとなぜ安定になるのかを説明できる
- 共鳴効果が説明に利用される現象を問題として作成できる
- 混成軌道に関連する知識
- 曲がった矢印
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に
「理解でつなぐ大学有機化学」をかわいくお届けします。

知識が本当に定着しているかどうかを確かめる方法の一つは、その知識を使って自分で問題を作ってみることです。
問題を解くときには、すでに用意された問いに答えればよい。
けれども問題を作るときには、何が本質で、どこでつまずきやすく、どの知識同士がつながっているかまで見えていなければなりません。
では、「共鳴を理解しているか」を測る問題を作るとしたら、何を問えばよいのでしょうか。
共鳴寄与体を書けること。安定な寄与体を選べること。
それだけでは、まだ十分ではありません。
共鳴は、酸性度、塩基性、結合長、反応性、反応点といった、有機化学のさまざまな現象に顔を出します。
だからこそ、共鳴を本当に使えるようになるためには、それがどこに現れ、何を変えているのかを整理しておく必要があります。
今回は、共鳴の基礎を復習しながら、
共鳴効果がどのような現象として現れるのかを分類して見ていきます。
自分ならどんな問題を作るか、そんな視点も頭の片隅に置きながら読み進めてみてください。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
文字が苦手な人も図を追えるように構成しているので、参考書のつもりでゆっくりどうぞ。
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
今日解説するポイントを確認

共鳴は、単に構造式を書き換えることができれば合格とはなりません。
電子が広い領域に非局在化した状態を読み取り、分子の性質や反応性を説明するための考え方です。
本記事では、共鳴を次の5つの視点から整理します。
- 電子は広い領域に分布することで安定化する(電子の非局在化)
- 共鳴寄与体の安定性が、実際の分子(共鳴混成体)の性質を決める
- 共鳴は電荷や孤立電子対を安定化させる
- 共鳴は結合の性質(結合長・回転障壁)を変化させる
- 共鳴は反応性や反応位置を変化させる
この5つを一つの流れとして整理すると、共鳴が有機化学のさまざまな現象を説明する共通の視点であることが見えてきます。
電子は広い領域に広がることで安定化する
π結合はp軌道がつくる広がりのある結合
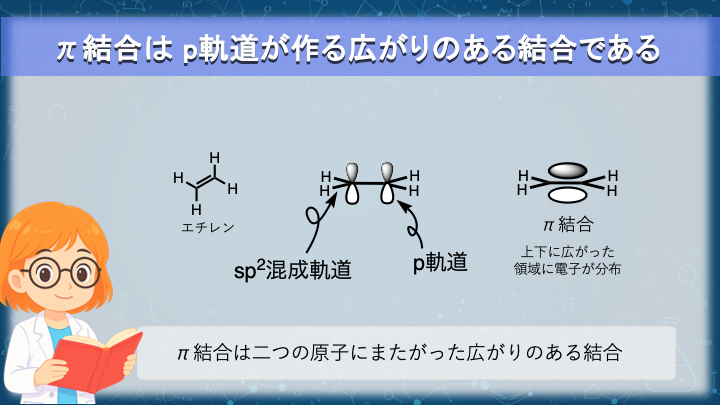
共鳴の話に入る前に、アルケンのπ結合を復習しておきます。
アルケンの炭素は sp² 混成しており、三本のσ結合を同一平面上に作ります。
このとき使われずに残る p 軌道が、平面に対して垂直方向に一つずつ存在します。
隣り合う炭素の p 軌道が並行に並ぶと、それらは横方向に重なり合い、π結合を形成します。
ここで重要なのは、π結合の電子は一つの原子の周囲に局在しているわけではなく、二つの炭素の上側と下側に広がった領域に分布しているという点です。
つまり、π結合とは二つの原子にまたがった広がりのある電子分布なのです。
では、このような p 軌道が二つではなく、三つ、四つと連続して並んでいた場合、電子はどのように分布するのでしょうか。
次で見ていきます。
π結合が拡張した状態を共役という
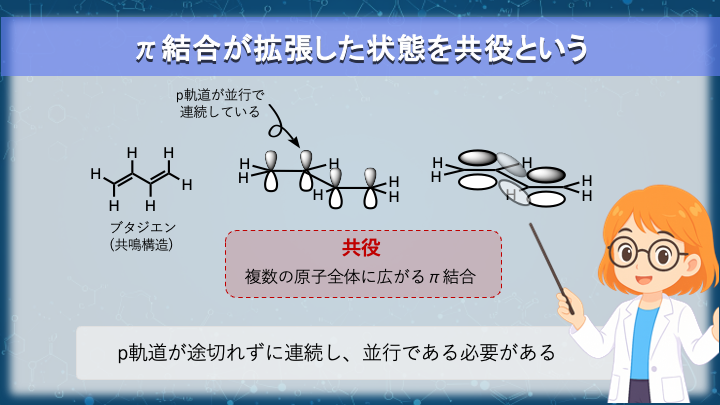
前節では、π結合の電子が二つの原子にまたがった領域に分布することを確認しました。
では、このような p 軌道が二つではなく、三つ、四つと連続して並んでいた場合はどうなるでしょうか。
p 軌道が連続しており、かつ互いに並行に並んでいるとき、それらの軌道はすべて横方向に重なり合うことができます。
このように p 軌道が連続してつながった状態を 共役 と呼びます。
共役している系では、π電子は二つの原子の間に局在するのではなく、連続した複数の原子にまたがって分布することになります。
例えばブタジエンでは、四つの炭素がそれぞれ p 軌道を持ち、それらが連続して並んでいます。
その結果、二対の π 電子は四つの炭素全体に広がった状態になります。
このような電子の非局在化を、有機化学では 共鳴構造 を用いて表現します。
電子は不確定性原理により広い領域に広がると安定化する

ここまでで、π電子が複数の原子にまたがって広がることを見てきました。
では、なぜ電子はこのように広い領域に分布すると安定になるのでしょうか。
この振る舞いは、量子力学の 不確定性原理 によって説明することができます。
不確定性原理とは、粒子の位置を強く限定しようとすると、その運動量の不確定さが大きくなるという関係です。
つまり電子を狭い領域に閉じ込めるほど、電子の運動は激しくなり、エネルギーが高くなります。
逆に、電子が広い領域に分布できる場合、運動量の不確定さは小さくなり、結果としてエネルギーを下げることができます。
このため、電子は可能な限り広い領域に分布する方が安定になります。
共役系や共鳴構造では、π電子が複数の原子にまたがって非局在化します。
この電子の広がりこそが、共鳴による安定化の本質です。
カルボキシラートの結合長は同じである
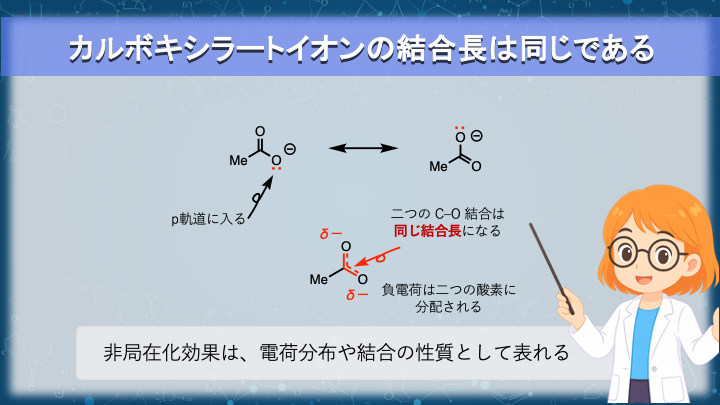
共役に参加する電子は、二重結合の π 電子だけではありません。
アニオンの電子やヘテロ原子の孤立電子対も、条件が整えば共役に参加します。
例えば水分子では、酸素の孤立電子対は sp³ 混成軌道に収容されており、特定の原子の周囲に局在しています。
しかしカルボキシラートイオンでは状況が異なります。
カルボニル基に隣接する酸素の孤立電子対は、p 軌道に入ることでカルボニルの π 系と重なり、共役に参加することができます。
その結果、負電荷は一つの酸素原子に局在するのではなく、カルボニル炭素と二つの酸素を含む領域に広がることになります。
特に二つの酸素原子の間で電子密度が分配されるため、カルボキシラートでは二つの C–O 結合の長さがほぼ等しくなることが知られています。
これは電子が二つの酸素に非局在化していることを示す実験的な証拠です。
共鳴寄与体に関する復習・安定性比較
共鳴寄与体と共鳴混成体
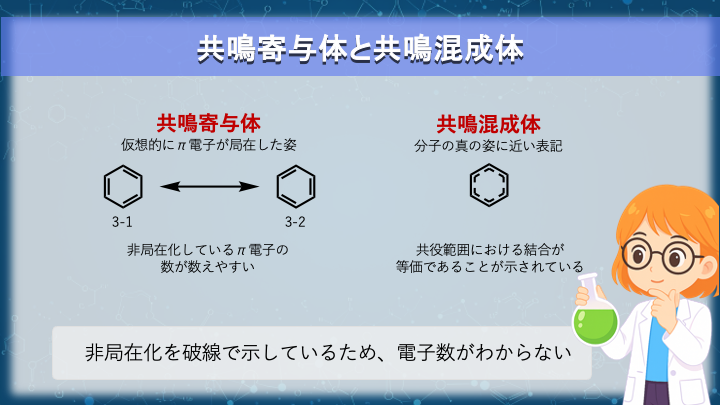
例えばベンゼンを書くとき、図に示す 3-1 や 3-2 のような構造式がよく用いられます。
これらの構造は、二重結合と単結合が交互に並んだ形を表しています。
しかし実際のベンゼンでは、三つの C=C 結合と三つの C–C 結合が存在しているわけではありません。
六つの炭素原子の p 軌道が連続して重なり、π電子は環全体に広がっています。
そのため、図 3-1 や 3-2 の構造は、ベンゼンの「実際の姿」を表しているわけではなく、電子の分布を表現するための 共鳴寄与体 と呼ばれる近似構造です。
実際の分子はこれらの構造のどちらかではなく、それらの特徴を合わせ持った 共鳴混成体 として存在します。
このとき、電子はベンゼン環全体に非局在化しているため、図では環の上に破線の円として表されます。
一方で、この表現では π 電子の数が直接示されません。
そのため電子数や電子の動きを考えるときには、π電子の配置が明確な共鳴寄与体の構造がよく用いられます。
共鳴寄与体はすべて同じ重要度を持つわけではありません。
より安定な寄与体ほど、共鳴混成体への寄与が大きくなります。
そのため構造式を代表として描くときは、最も安定な寄与体を主体に描くのが一般的です。
共鳴が起こる条件
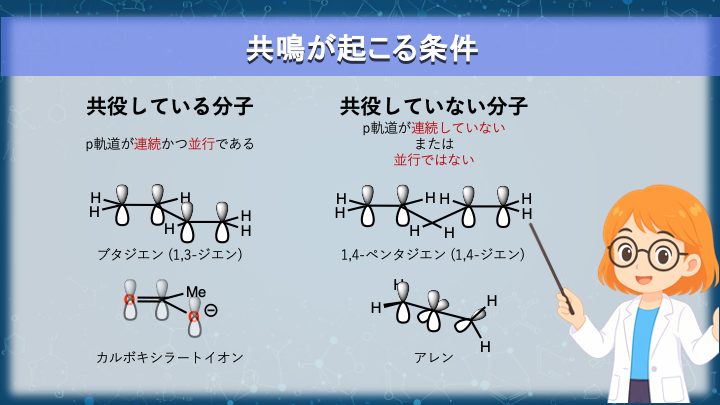
共鳴が起こるためには、p軌道が並行に連続していることが必要です。
p軌道が並行に並ぶと、それらの軌道が互いに重なり、π電子は複数の原子にまたがって広がることができます。
このように電子が複数原子に広がる状態を共役と呼びます。
例えばブタジエンのようなポリエン系では、すべての炭素が p 軌道を持ち、それらが連続して並んでいるため、π電子は4つの炭素原子に広がることができます。
三重結合を含む場合でも同様です。
三重結合には二つの π 結合がありますが、そのうち一つが隣接する p 軌道と並行になれば、共役に参加することができます。
また、二重結合に隣接するヘテロ原子の孤立電子対も、p 軌道に収容されることで共役に参加することがあります。
一方で、p軌道が連続していない場合の共役は起こりません。
例えば 1,4-ペンタジエン のように、二重結合の間に sp³ 炭素が挟まる場合、π系は途中で途切れてしまいます。
さらに、アレンも間違えやすい例です。
アレンでは二つの二重結合が一つの炭素を共有していますが、それぞれの π 結合は互いに 直交 しています。
そのため p 軌道は連続していても重なり合うことができず、共役系にはなりません。
共鳴寄与体の書き方:4つのルール
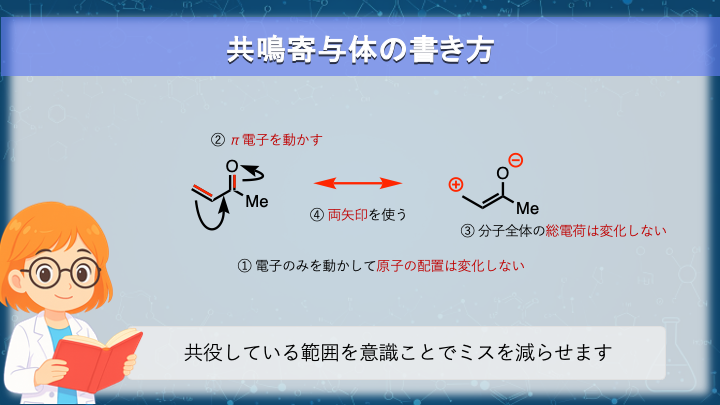
反応性を考察したり電子分布を理解したりするためには、共鳴寄与体を描いて電子の広がりを確認する必要があります。
共鳴寄与体を書くときは、次のルールに従います。
① 電子のみを動かす。原子は動かさない
共鳴は電子の分布の違いを表すものであり、原子の位置は変わりません。
② 動かせるのは π 電子または孤立電子対のみ
σ結合は骨格を作る結合なので、共鳴では動かしません。
③ 分子全体の電荷は変化しない
共鳴寄与体は同一分子の別表現なので、総電荷は必ず同じになります。
④ 曲がった矢印で電子の動きを示す
また、二つの構造が共鳴関係にあることは両矢印(↔)で示します。
共鳴構造を示すときに、片矢印(→)や平衡矢印(⇌)を使ってしまうミスがよく見られます。
共鳴は反応や平衡ではなく、同一分子の電子分布の表現なので両矢印(↔)を用います。
共鳴寄与体の安定性が分子の性質を決める
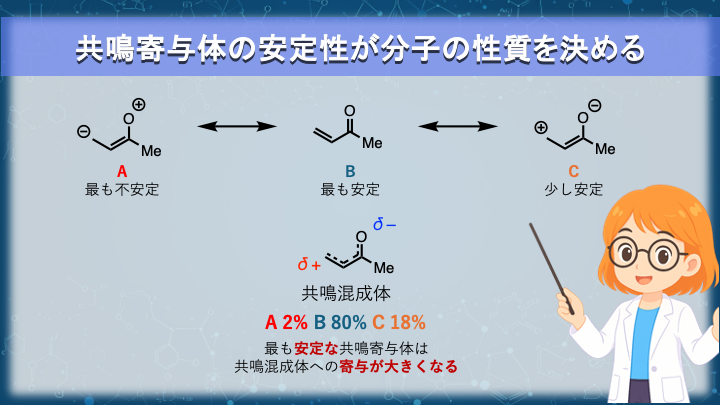
実際の分子は、共鳴寄与体のいずれか一つの構造ではなく、それらの特徴を合わせ持った 共鳴混成体 として存在します。
ただし、すべての共鳴寄与体が同じ割合で寄与するわけではありません。
共鳴混成体への寄与の大きさは、それぞれの共鳴寄与体の安定性に依存します。
より安定な共鳴寄与体ほど寄与が大きく、その特徴は実際の分子の性質に強く反映されます。
したがって、共鳴寄与体をすべて書き出し、それぞれの安定性を比較することで、
- 電荷がどこに分布するのか
- 結合がどの程度強くなるのか
といった分子の性質を考えることができます。
共鳴寄与体の安定性を評価する3つの基準
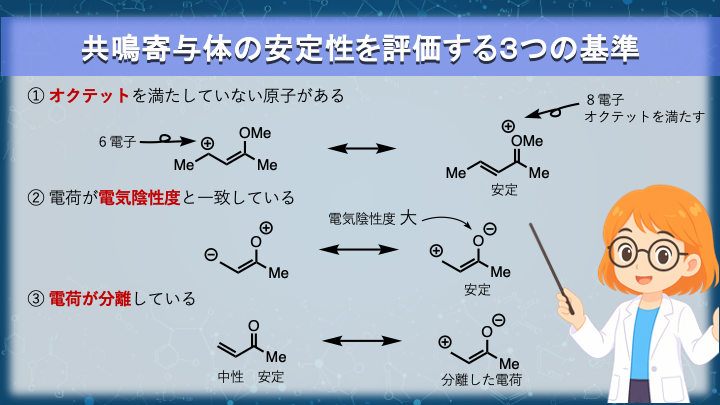
共鳴寄与体の安定性は、次の3つの基準で評価することができます。
重要度の高い順に並べています。
① オクテットを満たしていない原子がある
オクテット(8電子)を満たしていない原子を含む構造は不安定であり、共鳴混成体への寄与は小さくなります。
例えばカルボニル酸素から π 電子を抜き取ると、酸素がオクテットを満たさない オキセニウムイオン が生じます。
このような構造は不安定であり、寄与は小さくなります。
② 電荷が電気陰性度と一致している
電気陰性度は電子を引きつける強さを表す尺度です。
電気陰性度の大きい原子は負電荷を安定化し、電気陰性度の小さい原子は正電荷を安定化します。
そのため、負電荷が電気陰性度の大きい原子にあり、正電荷が電気陰性度の小さい原子にある構造ほど安定になります。
ただし、オクテットを満たさない構造よりは、オクテットを満たす構造の方が優先されます。
③ 電荷が分離している
正電荷と負電荷が分離した構造は、
静電エネルギーの観点から不安定になります。
そのため中性分子では、電荷が分離していない共鳴寄与体の方が安定です。
三つの基準をまとめます。
① オクテットを満たしていない原子がある
② 電荷が電気陰性度と一致していない
③ 電荷が分離している
これらは上から順に不安定化の影響が大きい要因です。
共鳴寄与体のまとめ
共鳴寄与体の基礎をまとめます。
- 電子は不確定性原理により、広い領域に広がると安定化する
- 共鳴寄与体は電子の動きだけを表し、原子は移動しない
- 共鳴混成体への寄与は、共鳴寄与体の安定性によって決まる
したがって、有機化学では共鳴寄与体を書くだけでなく、その安定性を比較することが重要になります。
共鳴効果が現れる現象
ここまでで、共鳴に関する基礎的な考え方を復習してきました。
ここからは、その共鳴が 実際の化学現象にどのように現れるのか を見ていきます。
共鳴は、多くの問題で登場する重要な概念ですが、問題を見たときに「共鳴を使う」と判断するのは意外と難しいものです。
そこで一度、立場を逆にして考えてみましょう。
問題を解くのではなく、「共鳴を使う問題」を自分で作るとしたら、どんな現象が題材になるでしょうか。
これまで問題演習を多く解いてきた人は、過去に見た問題を思い出せるかもしれません。
また、教科書を丁寧に読んできた人は、共鳴に関する様々な例を思い浮かべることができるはずです。
この「問題を作る」という操作は、知識を単なる理解から 使える知識 へと引き上げます。
ここからは、共鳴効果がどのような現象として現れるのかを整理していきます。
それでは見ていきましょう。
アニオン安定化と酸性度
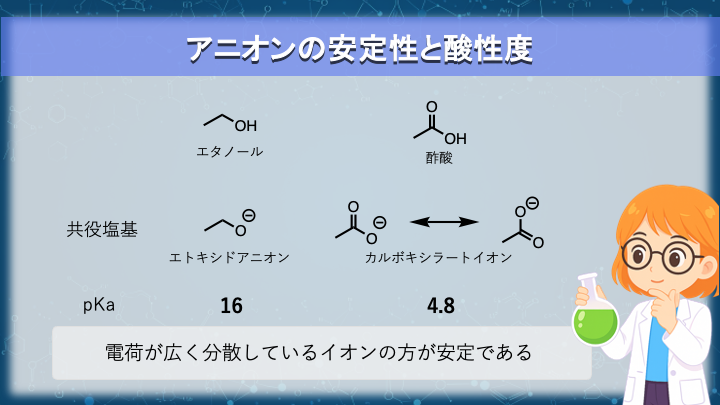
電子の非局在化は、アニオンの安定性を考えるときに最もよく登場する概念です。
図の問題では、エタノールと酢酸の酸性度を比較しています。
酸性度を比較するときには、共役塩基(酸がプロトンを失った後のアニオン)の安定性を考えるのが基本です。
これは酸塩基反応が平衡反応であり、平衡の位置が生成物と反応物の熱力学的安定性によって決まるためです。
エタノールの共役塩基は エトキシドアニオン であり、負電荷は酸素原子上に局在しています。
一方、酢酸の共役塩基は カルボキシラートイオン です。
このイオンではカルボニル基と共役することで共鳴が起こり、負電荷は二つの酸素原子に非局在化します。
このように電荷が複数の原子に分散すると、静電エネルギーが低下して分子は安定化します。
その結果、酢酸の共役塩基の方が安定となり、酢酸はエタノールよりも強い酸になります。
(pKaはエタノール ≈ 16、酢酸 ≈ 4.8)
酸性度は、求核性や脱離基の脱離能とも密接に関係します。
これらの性質を問う問題でも、共鳴による電荷分散が重要な判断材料になります。
電荷分布と塩基性
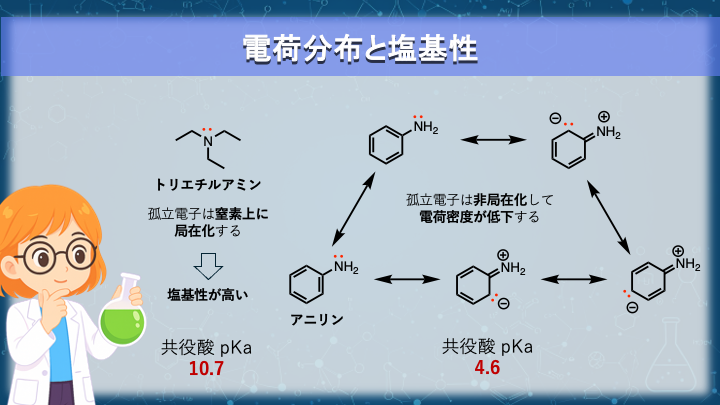
塩基性を比較する際にも重要な要因になります。
図では、アニリンとトリエチルアミンの塩基性を比較しています。
塩基として働くとき、
反応の中心となるのは 窒素上の孤立電子対 です。
塩基はこの電子対を用いて H⁺ と結合します。
トリエチルアミンでは、この孤立電子対は窒素原子上に局在しています。
一方、アニリンでは窒素の孤立電子対がベンゼン環の π 系と共役することができます。
その結果、電子はベンゼン環にも広がり、窒素上の電子密度は低下します。
電子密度が低下すると H⁺ を引きつける力も弱くなるため、
アニリンはトリエチルアミンよりも弱い塩基になります。
共鳴による結合長の平均化
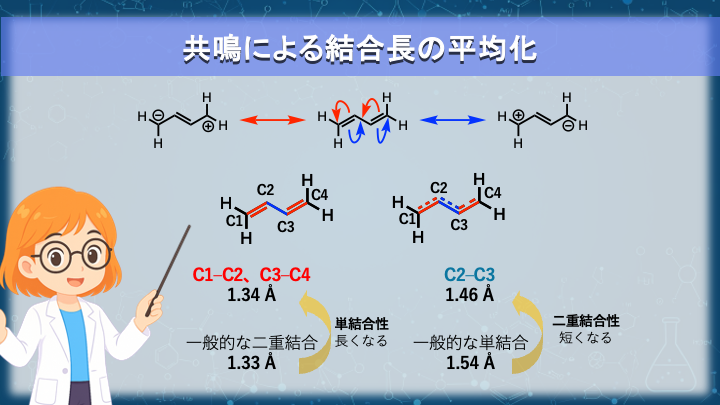
共鳴は、分子の安定性だけでなく、結合長などの物理的な性質にも影響を与えます。
例えばブタジエンでは、中央の C2–C3 結合は単結合として描かれます。
しかし実際に測定すると、この結合は通常の単結合よりも短くなっています。
これは共鳴によって、中央の結合が部分的に二重結合の性質を持つためです。
同様に、端の二重結合は通常のアルケンの二重結合よりもわずかに長くなります。
つまり共役系では、単結合と二重結合の区別が完全ではなくなり、結合次数が平均化された状態になります。
実際にブタジエンの C2–C3 結合は通常の単結合(約1.54 Å)より短い約1.46 Å と測定されています。
ペプチド結合の部分二重結合性と剛直性
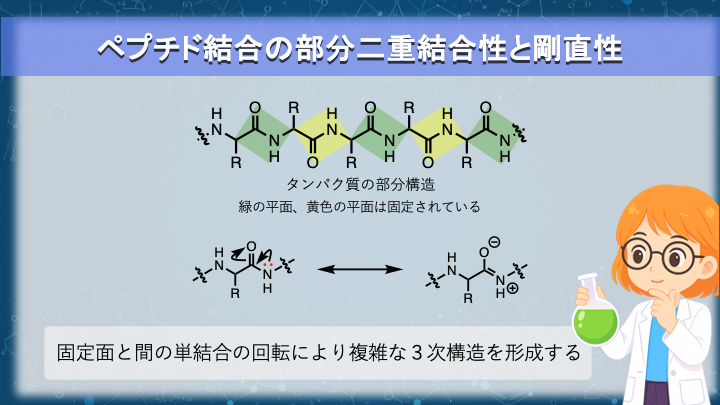
共鳴の影響は、結合の性質を変化させることがあります。
その代表的な例が ペプチド結合 です。
ペプチドでは、窒素原子がカルボニル基に隣接しています。
そのため窒素の孤立電子対はカルボニルの π 系と共役することができます。
この共鳴によって、カルボニル炭素と窒素の間の結合は 部分的な二重結合性 を持つようになります。
その結果、
- C–N 結合は通常の単結合より短くなる
- C–N 結合の回転が強く制限される
という特徴が現れます。
つまりペプチド結合では、窒素の置換基とカルボニル基は ほぼ同一平面上に固定されます。
この結合の剛直性はポリペプチドにも引き継がれ、タンパク質の三次元構造を形成する際の重要な要因となります。
例えばタンパク質では
- αヘリックス
- βシート
といった構造が形成されます。
これらの構造は水素結合によって安定化されますが、その前提として ペプチド結合の平面性と剛直性 が重要な役割を果たしています。
アミド結合の回転障壁は約20 kcal/molと大きく、常温ではほとんど自由回転しません。
これも共鳴による部分的な二重結合性で説明できます。
アリル位の反応性と電子の非局在化
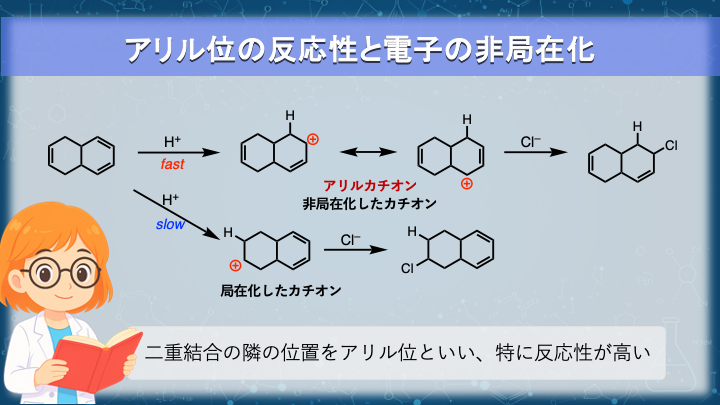
共鳴効果は、分子の安定性だけでなく、反応性にも影響を与えることがあります。
図の問題では、共役ジエンと孤立したアルケンの二つの反応部位を持つ分子に対して、塩酸を付加させています。
どちらのアルケンにプロトンが付加した場合でも、生成するカルボカチオンは第二級となります。
したがって、単純な置換基効果だけでは反応部位の違いを説明することができません。
ここで重要になるのが 共鳴効果 です。
アルケンに隣接した位置は アリル位 と呼ばれます。
この位置にカルボカチオンが生成すると、正電荷は隣接する π 結合と共鳴することができます。
このようなカチオンを アリルカチオン と呼びます。
アリルカチオンでは正電荷が複数の原子に非局在化するため、通常のカルボカチオンよりも強く安定化されます。
その結果、このカチオンを経由する反応では中間体や遷移状態のエネルギーが低下し、反応はこの経路を優先して進行します。
つまり、アリル位の反応性が高いことは共鳴によるカチオンの安定化で説明することができます。
アリル位やベンジル位の反応性が高いのは、共鳴によって中間体が安定化されるためです。
そのため求電子付加だけでなく、ラジカル反応や求核置換反応でも重要な概念になります。
電子密度分布が反応点を決める(1,4付加・芳香族求電子置換)
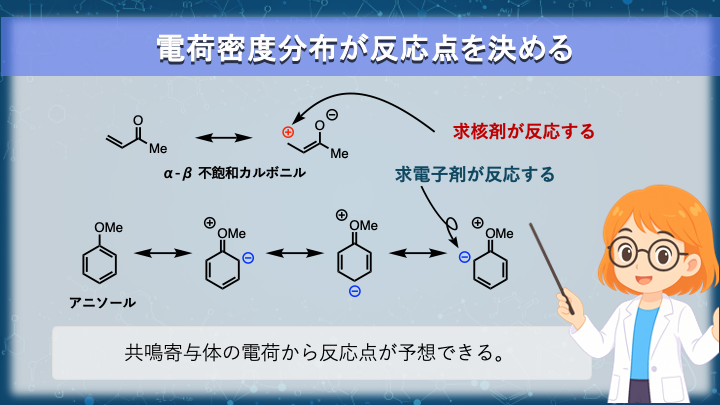
共鳴効果は分子の安定性だけでなく、電子密度の分布を変化させます。
その結果、分子の 反応点 が変わることがあります。
例えば、通常のアルケンは電子が豊富なため、求電子剤と反応することができますが、
求核剤を受け入れることはほとんどありません。
しかし、アルケンがカルボニル基と共役したα,β不飽和カルボニル化合物になると状況が変わります。
この分子では共鳴寄与体を書くことで、β炭素に部分的な正電荷が生じていることが分かります。
つまり、共鳴によって電子密度が偏ることでβ位が求核剤の攻撃を受けやすい反応点になります。
このため、α,β不飽和カルボニルではβ位での 1,4付加反応 が起こることがあります。
同様の考え方は、芳香族求電子置換反応の位置選択性の説明にも用いることができます。
例えばメトキシ基を持つアニソールでは、共鳴寄与体を書くと芳香環の オルト位とパラ位 に負電荷が現れます。
これは共鳴混成体においてこれらの位置の電子密度が高いことを意味します。
その結果、求電子剤はオルト位やパラ位で反応しやすくなります。
共鳴は電子密度の分布を変えるため、「どの位置が反応しやすいか」を決める重要な要因になります。
この考え方は1,4付加反応や芳香族求電子置換反応など、多くの有機反応の理解に使われます。
まとめ
最後に本記事の主張をまとめます。
- 電子は不確定性原理により広い領域に広がると安定化する
- 共鳴寄与体の安定性は、共鳴混成体への寄与の大きさを決め、分子の性質に影響する
- 共鳴は電荷や孤立電子対を分散させ、分子を安定化する
- 共鳴は結合の性質(結合長や回転障壁など)を変化させる
- 共鳴による電子密度の変化は、反応速度・選択性・反応位置に影響を与える
終わりに
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
今回は共鳴について解説しました。
どんな分野の学習でも、作問してみることは理解を深める良い方法です。
ぜひ一度、自分で問題を作るつもりで考えてみてください。
次回は 芳香族性 について解説していきます。
保育園の頃の記憶はほとんど残っていませんが、
妹が保育士なので、どんな仕事をしているのかよく話を聞きます。
「みんなで手をつないで輪になって」
「おもちゃは独り占めしないでみんなで使おうね」
そんな話を聞くたびに思います。
日本人は保育園の頃から芳香環の英才教育を受けていたのかもしれません。
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック




コメントを残す コメントをキャンセル