- 互変異性化を平衡の基礎から説明することができる
- ケトン側に平衡が偏る理由を説明できる
- 酸性条件・塩基性条件での互変異性化の反応機構を書くことができる
- 反応速度論に関する基礎知識
- アルケン、アルキンの求電子付加反応
- 反応機構を書くための基礎知識
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に
「理解でつなぐ大学有機化学」をかわいくお届けします。
ケト–エノール互変異性化は、「ケトンになる反応」として処理されることが多い現象です。
実際、多くの反応機構では、最終生成物としてケトンだけが描かれます。
「互変異性化」を固有名詞として終わらせるか、それとももっと大きな枠組みの中で解釈し、応用するかはたった一つの簡単な視点を持てるかで変わります。
この記事では、互変異性化を特別扱いするのではなく、“化学平衡の一例”として見直していきます。
なぜ、ケトンが優先されるのか、生成物のバランスを決めている安定性から解説していきます。
後半では、アルキンの水和反応を題材に、実際の反応の反応機構ではどんな落とし穴があるのか確認します。
今回は、互変異性化を覚える話ではありません。
平衡と安定性という物差しで、反応を考え直すことを目標とします。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を今日も一緒に見ていきましょう。
文字が苦手な人も図を追えるように構成しているので、
参考書のつもりでゆっくりどうぞ。
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
この記事でわかること:ケト–エノール互変異性はどちらが安定か

今回の講義では、“ケトエノール互変異性化のバランスを決めるのは何か”という部分を中心に解説していきます。
まず意識してほしいのは、ケト–エノール互変異性化は“速く進行する平衡反応の一例である”ことです。
平衡は偶然で決まるのではなく、そこに並ぶ化学種の安定性の差がバランスとして現れます。
この視点で眺めると、C=C をもつ構造とC=O をもつ構造のどちらに偏りやすいかが見えてきます。
また、互変異性化は酸や塩基の存在によって進み方が変わります。
反応条件は、後で機構を考えるときの重要な手がかりになります。
まず初めの章であるここでは、以降の議論で使われる平衡・安定性・液性条件の三つのキーワードを軽く心に留めておいてください。
全て読み終わった後ここに戻ってくると、より深く今日のポイントを刻むことができます。
ケト–エノール互変異性は「速い平衡反応」として考える
平衡反応とは何か:正反応と逆反応が同時に進む状態
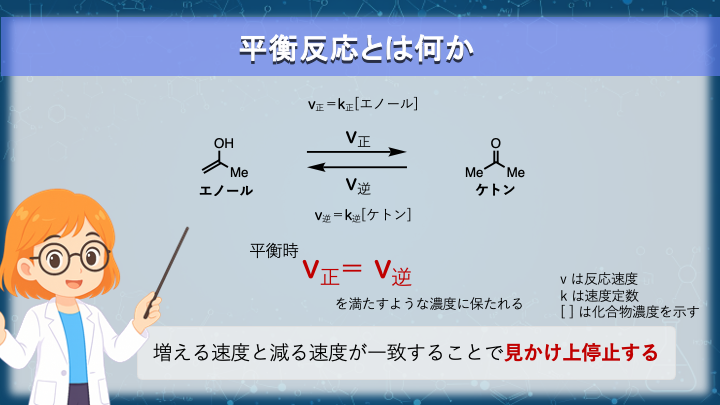
互変異性化とは二つの構造異性体が “速い平衡” で共存する状態を言います。
平衡反応とは、 正反応 と 逆反応 が同時に進行している反応系のうち、その反応速度が等しくなった状態を指します。
この状態では、分子の変換は止まっていません。
進む向きと戻る向きが同じ速さで起きているため、見かけ上、組成が変化しなくなります。
速度論の言葉では、正反応の速度と逆反応の速度が等しくなる濃度関係として表され、
v正 = v逆
が成り立つとき、反応系は平衡にあります。
互変異性化では相互変換が非常に速いため、この平衡状態にほぼ瞬時に到達します。
図では、平衡状態の速度論的な定義を図示しています。
正反応と逆反応の釣り合い位置の濃度に保たれるというイメージを大切にしましょう。
数式の厳密な理解は後回しでも理解できる記事にしてあります。
次に、少し寄り道して平衡定数とは何か感覚的に掴んでみましょう。
平衡定数は「どちらが多く存在するか」を表す指標
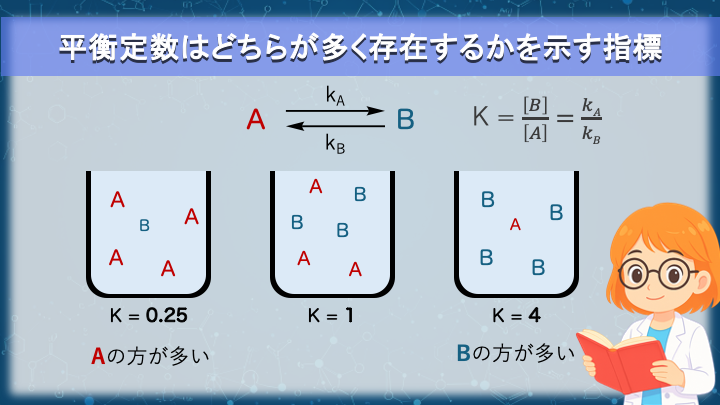
平衡定数は、反応がどちらにどれだけ偏っているかを示すための指標であるとも言えます。
基準になるのは K=1 という値です。
K=1 のとき、反応系には左右の化学種が同程度存在しています。
ここから、K が大きくなるほど右側の化学種が多くなり、小さくなるほど左側の化学種が多くなります。
一見すると、元に戻らないように見える反応でも、実際には極端に偏った平衡反応である例は少なくありません。
ケト–エノール互変異性化でも、最終生成物としてケトンだけを描くのは、平衡がケトン側に大きく偏っているためです。
図では、AがBになる平衡反応の平衡定数が1の時、1より小さい時、1より大きい時を仮定して、フラスコの中の状態がどうなっているのかを図示しています。
次では、この偏りが何によって決まるのかを考えていきます。
平衡がどちらに偏るかは、化学種の安定性で決まる
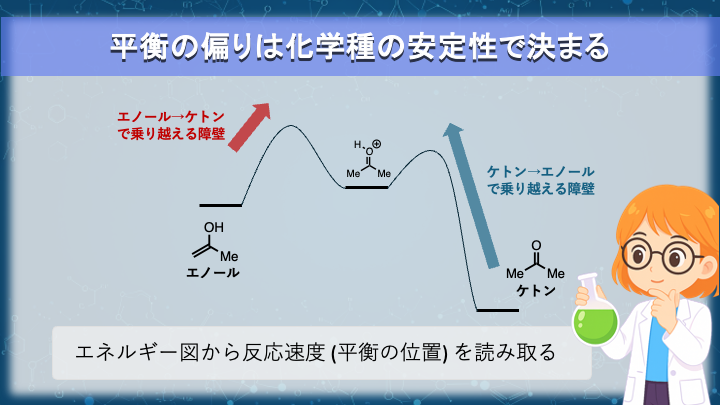
平衡定数は、正反応と逆反応の速度定数の比として定義されます。
ここで重要なのは、数式そのものではなく、この比が「どちらの変換が起こりやすいか」という傾向を表している点です。
分子の相互変換が繰り返される反応系では、より安定な化学種から別の形へ変わる変換は起こりにくくなります。
一方で、不安定な化学種から安定な化学種へ向かう変換は、比較的起こりやすくなります。
図では不安定なエノールからより安定なケトンに変換されるときのエネルギー図を示しています。
正反応と逆反応の活性化自由エネルギーを比較すると、逆反応の方の登り坂が長いことがわかるはずです。
この変換の起こりやすさの差が積み重なった結果として、平衡に達したとき、反応系にはより安定な化学種が多く存在する状態が保たれます。
平衡の位置とは、この安定性の差が分子の数として表れた姿に他なりません。
ケト–エノール互変異性化が一般にケト体側へ偏って見えるのも、ケト体がより安定な化学種であるためです。
平衡反応といえば安定性の議論。
この考え方は、この反応に限らずに多くの可逆反応に応用できます。
一般にケト体が安定な理由:結合エネルギーの違い
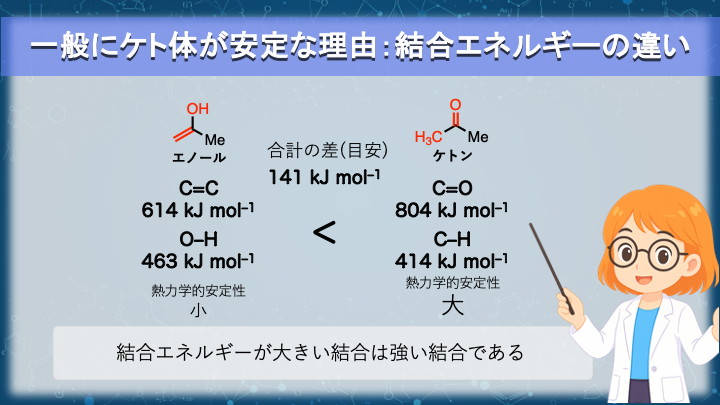
互変異性化を納得して理解するためには、なぜケトンが安定になりやすいのかを、一度、直感的なレベルで整理しておくと役に立ちます。
ここでは化合物の安定性を、含まれる化学結合の強さから大まかに見積もります。
これは厳密な理論ではなく、「どちらが安定になりやすいか」を掴むための近似です。
エノールとケトンを比べると、二重結合の位置と、水素が結合している原子が異なっています。
図では、C=O と C=C、O–H と C–H を、結合エネルギーの観点で比較しています。
一般に、C=O 結合は C=C 結合より強く、O–H 結合は C–H 結合よりも強いと知られています。
このような結合を多く含む構造は、全体としてエネルギー的に安定になりやすいと考えられます。
多くの場合、ケト体はエノール体よりも強い結合を多く含む構造をとるため、より安定になりやすいと推測できます。
これが、ケト体側に平衡が偏る理由を直感的に説明する一つの見方です。
この説明は便利ですが近似です。
別の要因で、例外的にエノールが安定な場合が存在します。なぜ安定化されているのかが重要です。
エノール体が優先されるのはどんなときか?
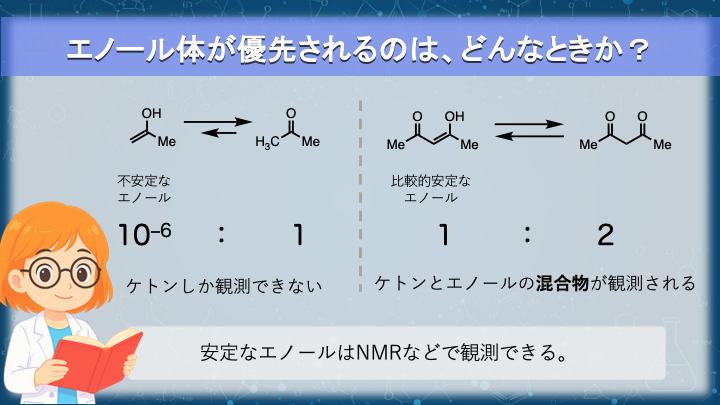
平衡の位置は、常に「どちらの化学種がより安定か」で決まります。
これは、ケト体が有利な場合でも、エノール体が有利な場合でも同じです。
通常の系では、ケト体とエノール体の比はおよそ 1:10⁻⁶ 程度となり、分析的には一種類の化合物として観測されます。
しかし、エノール体が特別に安定化される条件では、この平衡は別の位置に移動します。
エノール構造が観測されるかどうかの分かれ目は、エノール体がどの程度安定化されているかにあります。
平衡がケト体側に強く偏るか、それともエノール体が無視できない割合で存在するかは、この安定性の差によって決まります。
有機化学の研究では、NMR 測定でケト体とエノール体の両方のピークが観測される例があります。
単離後であっても平衡に戻るのは、互変異性化が速い可逆反応だからです。
1,3-ジケトンのエノール体が安定な理由(分子内水素結合と共役)
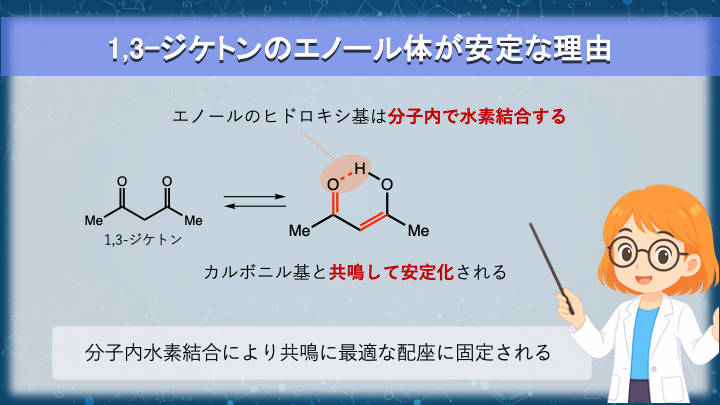
1,3-ジケトンは、エノール体が無視できない割合で観察される代表的な化合物です。
これは、前節で見た「安定な構造が平衡で優先される」という原理を、具体的な分子構造で確認できる例です。
1,3-ジケトンとは、二つのカルボニル基が一炭素を挟んで並ぶ骨格をもつ化合物です。
この構造では、エノール体になることで、C=C 結合と C=O 結合が連続して配置されます。
その結果、共役による電子の非局在化が生じ、エノール体は単純なエノールよりも安定化されます。
さらに、エノール体では分子内水素結合が形成されます。
この水素結合は、構造を固定することでカルボニル基とエノール部位を同一平面上に保ち、共役による安定化をさらに強めます。
このように、共役安定化と分子内水素結合という二つの安定化要因が同時に働くことで、エノール体の熱力学的安定性は大きく高まります。
その結果、平衡はエノール側へと偏るのです。
平衡のバランスの本質は“安定性”、例外的なエノールも安定性の軸で理解することで、より応用できる理論として整理することができます。
フェノールがケト体にならない理由:芳香族安定化
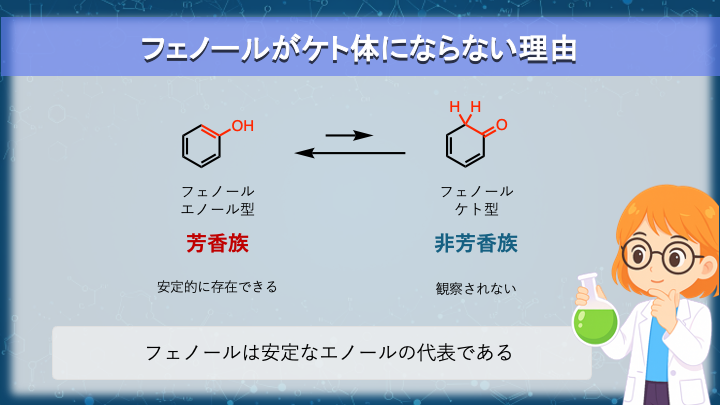
これまで見てきたように、平衡の位置は「どちらの構造がより安定か」によって決まります。
エノール体が優先されるかどうかも、例外ではなく、この原理に従っています。
フェノールは、有名な芳香族アルコールとして知られていますが、互変異性化の視点で見ると、極めて強く安定化されたエノール体であると解釈できます。
図では、フェノールのエノール体と仮想的なケト体を並べています。
ケト体を描くことは可能ですが、芳香族性を失うため著しく不安定になります。
この安定性の差は、1,3-ジケトンで見た共役や水素結合をはるかに上回るものです。
芳香族安定化が支配的に働くため、平衡は事実上エノール側に完全に偏ります。
その結果、フェノールではケト体は観察されません。
フェノールは、「エノールは不安定である」というイメージを根本から書き換えてくれる化合物だと言えます。
平衡反応といえば“安定性”の議論である。とても大切な考え方です。
ここまでの整理:互変異性化は「安定性」で理解できる
- ケト–エノール互変異性化は、特別な反応ではなく速い平衡反応の一例である
- 平衡でどちらが多く存在するかは、化学種の安定性によって決まる
- 多くの場合はケト体が安定だが、構造によってはエノール体が優先することもある
ここまでの話は、「互変異性化をどう覚えるか」ではなく、「どう解釈するか」を整えるためのものでした。
次の章では、この見方を使って、実際に反応機構を書いていきます。
ケト–エノール互変異性は酸性条件と塩基性条件で機構が変わる
ケトエノール互変異性化は酸や塩基によって触媒されて進行します。
反応機構を書く際に一つ注意する必要があります。
それは、酸性と塩基性で経由する中間体が異なるということです。
次節からそれぞれの反応機構をまずは解説していきます。
酸性条件では、正電荷をもつ中間体が中心となる

酸性条件の反応機構を書くとき、最初に確認すべきなのは「どのような電荷を持つ中間体が存在しうるか」です。
酸性条件では、反応系全体がプロトン供与的な環境にあります。
この環境では、電子対を受け取る側(カチオン)は存在しますが、電子対を過剰に抱えた化学種(アニオン)は安定に存在できません。
そのため、酸性条件下の反応機構では、正電荷を持つ中間体、または中性中間体のみを経由します。アニオン中間体が現れる余地はありません。
エノールからケト体への変換を例に見てみましょう。
エノールでは、酸素の孤立電子対がカルボニル形成に使われ、同時に α 位がプロトン化されます。
この段階では、酸素上のプロトンはまだ外れていないため、分子全体として正電荷を持つオキソニウムカチオンが生成します。
その後、脱プロトン化が起こり、中性のカルボニル化合物へと落ち着きます。
酸性条件で描かれる中間体は、常に「電子を余分に持たない形」である、という点を意識して機構を書いていきましょう。
反応機構を書く前に液性を見る。これは、この章全体を通して使う大切な視点です。
塩基性条件では、負電荷をもつ中間体が中心となる
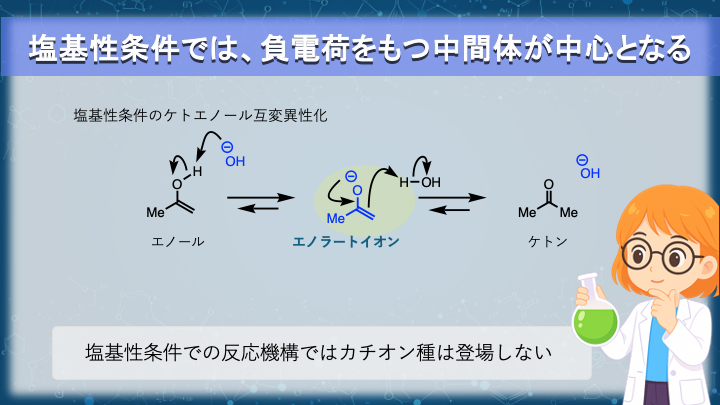
塩基性条件では、反応機構の考え方が酸性条件とは根本的に異なります。
この条件では、反応系全体がプロトンを奪う側にあり、電子対を過剰に抱えた化学種(アニオン)が安定に存在できます。
そのため、塩基性条件下の反応機構では、負電荷を持つ中間体、または中性中間体のみが現れます。正電荷を持つ中間体が中心となることはありません。
ケト–エノール互変異性化では、まず水酸化物イオンがエノールの OH からプロトンを引き抜き、エノラートイオンが生成します。
続いて、エノラートの電子対がカルボニル形成に使われ、同時に α 位でプロトンが供給されます。
このときのプロトン源は、酸性条件のような H₃O⁺ ではなく、中性の水分子です。
結果として、水酸化物イオンが再生され、塩基は触媒として機能します。
塩基性条件では、アニオンが中心の世界であり、プロトン移動は中性水分子とアニオンの間で起こります。
この視点を持つことで、酸性条件の延長で機構を書いてしまう誤りを避けることができます。
酸性でも塩基性でも、互変異性化は速い平衡反応である
酸性条件でも塩基性条件でも、ケト–エノール互変異性化の本質は変わりません。
いずれの場合も、この反応は速い平衡反応です。
反応機構の途中で現れる中間体の電荷は条件によって異なりますが、正反応と逆反応は常に同時に進行しています。
反応が止まって見えるのは、両者の速度が釣り合っているためです。
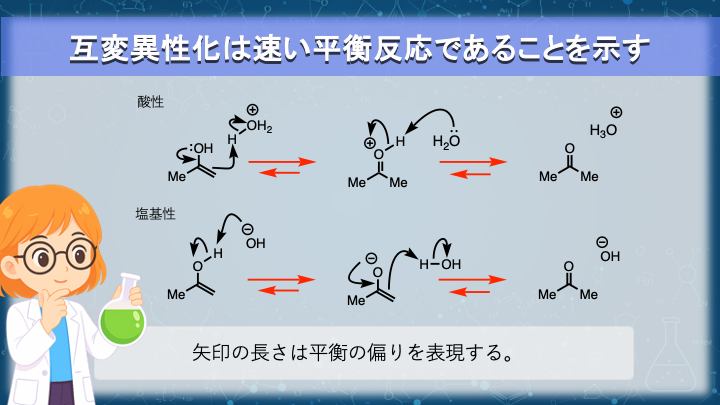
図では、酸性条件と塩基性条件の機構を並べて示しています。
どちらの条件でも、すべての変換が双方向の矢印で結ばれている点に注目してください。
この双方向性こそが、互変異性化が平衡反応であることを示しています。
矢印の長さは、平衡がどちらに偏っているかを表しているにすぎません。
矢印は単なる記号ではありません。 反応が「行き来している」ことを示す、大切な情報です。
アルキンの水和・ヒドロホウ素過酸化で起きる互変異性化
アルキン水和では、まず反応条件が酸性か塩基性かを確認する
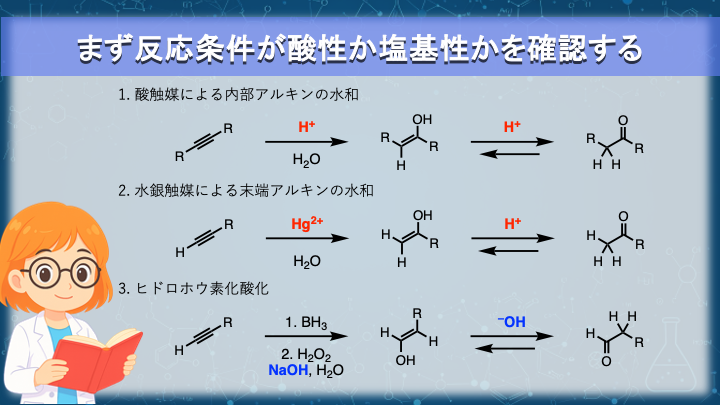
この章では、アルキンがいったん エノール を経由し、最終的に ケトン/アルデヒド として観測される代表例を並べます。
ここでの主役は「水和そのもの」ではなく、その後に必ず挟まる互変異性化を、どの液性で書くべきかです。
反応機構を書くときに、まず決めるべきことは一つだけ。
その反応条件が酸性か、塩基性かです。
- 酸性条件:カチオン(または中性)を中心に書く。アニオンを無理に出さない。
- 塩基性条件:アニオン(または中性)を中心に書く。カチオンを無理に出さない。
図では、この章で扱う反応を「酸性/塩基性」の軸で並べています。
この分類さえ最初に固定できれば、互変異性化で中間体の電荷を取り違えるミスは大幅に減ります。
反応機構を書くときは、酸性か塩基性かをまず初めに考える。
酸性条件で進む内部アルキンの水和反応
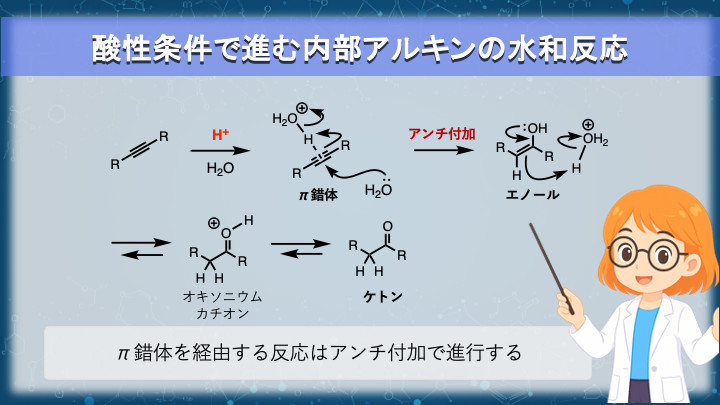
この水和反応の反応条件は、明確に酸性です。
そのため、反応機構はアルキンの π 電子系が部分的にプロトン化され、
π 錯体を経由して進行します。
この点は、#U10 で扱ったアルキンに対する HX 付加反応と共通しています。
いずれの場合も、反応の本質は「酸性条件下での求電子付加」です。
ここで注意したいのは、HX 付加で学んだ付加様式(アンチ付加)を、中間体であるエノールの構造にまで正しく適用できているか、という点です。
最終生成物がケトンになるからといって、エノール中間体の立体や結合関係を曖昧にしてしまうと、反応機構全体の整合性が崩れ、減点されてしまいます。
内部アルキンでは、アルキル基の電子供与効果により、このような求電子反応が進行しやすくなります。
一方で、末端アルキンでは同条件では反応が進みにくく、追加の触媒が必要になることもあります。
水銀触媒を用いる末端アルキンの水和(酸性条件)
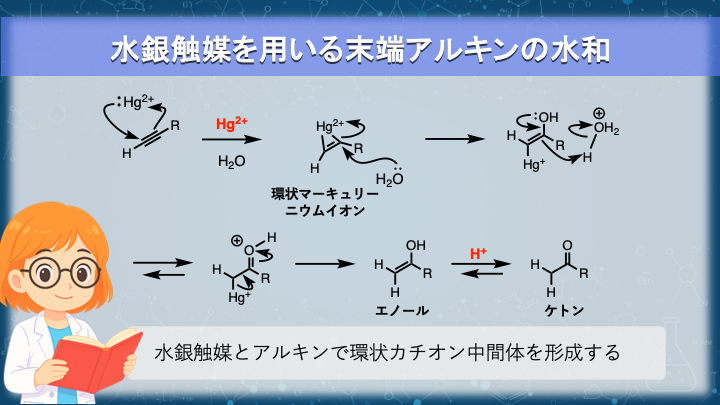
末端アルキンの水和反応は、水銀触媒を用いるため、特別な反応のように扱われることがあります。
しかし、この反応の液性は一貫して酸性です。
その理由は、水銀触媒そのものがカチオニックな性質を持つためです。
水銀触媒の存在下では、アルキンは環状マーキュリーニウムイオンを中間体として反応します。
この中間体は、ハロゲン分子 X₂ がアルケンと反応して生じる環状ハロニウムイオンとよく似た電子構造を持っています。
この環状中間体は正電荷を帯びており、求電子的に活性化された状態にあります。
その結果、水分子による求核攻撃が起こります。
求核位置は、部分正電荷の安定性に基づいて決まり、より安定な内部側が選択されます。
その後、脱メタル化を経てエノールが生成し、ケト–エノール互変異性化によって最終的にケトンが得られます。
環状ハロニウム・位置選択性については#U3で解説しています。
水銀触媒を使っていても、機構の判断軸は「酸性条件」で変わりません。
ヒドロホウ素化酸化 (塩基性条件)
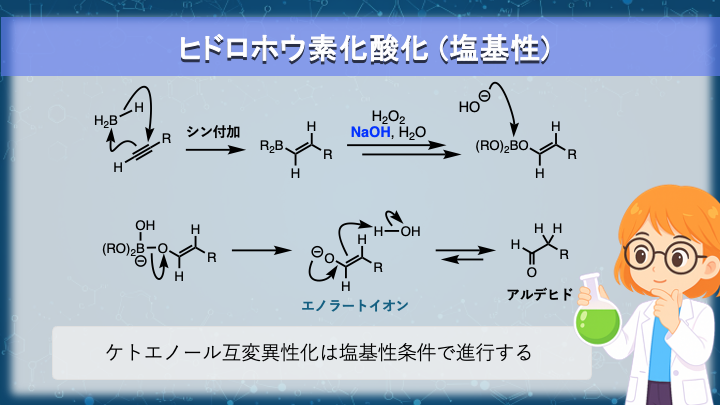
ヒドロホウ素化酸化は、アルキンに対しても進行する反応です。
この互変異性化における液性は、明確に塩基性です。
実際に、アルキン炭素に酸素置換基が導入されるのは、酸化工程の後半です。
この段階では、水酸化ナトリウムが用いられており、反応系は明確に塩基性条件に置かれています。
このため、生成したエノールは、酸性条件のようにオキソニウムカチオンを経由することはありません。
代わりに、エノラートイオンを経由した互変異性化として整理することができます。
ヒドロホウ素化から酸化に至るまでの付加様式そのものは、アルケンの場合と変わりません。
重要なのは、互変異性化が進行する条件が「塩基性側に固定されている」という点です。
その結果、ここでも反応機構の書き方は、「塩基性条件ではアニオン中間体のみを扱う」という原則に完全に従います。
酸性条件と塩基性条件は、混ぜてはいけません。同じ「水和」に見えても、反応系の性質はまったく異なります。
まとめ:ケト–エノール互変異性は平衡と安定性で理解する
今回は、ケトエノール互変異性化は“速い平衡である”ことを主軸にして、平衡反応の基礎から理由を考察し、実際の例で反応機構を書く際の注意点を述べてきました。
- ケト–エノール互変異性化は、速い平衡反応として常に進行しています。観察される姿は、平衡の結果にすぎません。
- 平衡反応の偏りは、それぞれの化学種の安定性で決まります。多くの場合、より安定な構造が多く存在します。
- 一般に、C=C結合よりもC=O結合は強い結合です。そのため、ケト体が安定になる傾向があります。
- 互変異性化は、酸や塩基によって触媒されます。反応条件に応じて、想定すべき機構は切り替わります。
- アルキンの水和反応では、いずれもエノールを経由します。最終的に、ケトンまたはアルデヒドが得られます。
終わりに
今日も有機化学のお勉強、お疲れさま〜〜( ̄▽ ̄)b☆
平衡反応という言葉を、高校以来ひさしぶりにじっくり考えた人もいるかもしれません。大学有機化学で登場する平衡反応はこれだけに収まりません。
また登場する際は、平衡のバランスを制御するためにどんな工夫があるのか注目していきたいですね!
さて次回は、“アルキンを自在に還元する方法”を解説していこうと思っています。
キーワードは“接触“と”溶媒和電子”です。
寒い冬は人肌恋しく感じますね。そんな時ふとした瞬間の”接触”にドキドキしてしまいます。
皆さんもドアノブを触る時は、気をつけましょうね!
静電気の力って結構侮れないですから。
あなたにとって、有機化学が少しでも笑える学問でありますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック





コメント