- Diels-Alder反応の反応機構を書き、位置選択を予想することができる
- endo体とexo体を見分けることができる
- シクロペンタジエンがなぜ高反応性なのかを説明できる
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に「理解でつなぐ大学有機化学」をかわいくお届けします。
やっほ〜🧪 博士課程有機化学研究生 aIRa(アイラ)です☆
専門書を何周も読んで見えてきた、“有機化学の本当の楽しみ方”を
今日も一緒に見ていきましょう。
皆さんは『効率』を意識して生活していますか?
料理でも勉強でも、少し工夫するだけで結果が大きく変わる。
有機化学の世界でもそれは同じで、C―C結合をどう効率よく作るかがとっても大切。
今日解説する「Diels-Alder反応」はC―C結合を同時に2つ形成できる
効率厨のファーストチョイス。
反応が発見されて100年近く経った今でも、最先端の研究で大活躍しています。
「6員環を作ればいいんでしょ?」、
「生成物の形がわかるからOK」
そんなふうに“なんとなく理解した気になって”、そのままにしていませんか?
実はこの反応、有機化学の基礎思考(電荷・共鳴・配座・軌道)の
使い方を学ぶ最強の練習台だったりします。
今回の講義は、ブルース教テンの理念に基づき、
“効率的な周回”を伝授します。
- #U6:入門編
できるだけ軌道を使わず、電荷・構造の直観で理解する - #U7:基礎編
フロンティア軌道論を導入して、同じ内容を別角度で理解する - #A12,13:応用編
実際に使われる設計・反応の戦略へ続く
というふうに同じ反応について、レベル別で分けて説明していきます。
読んでいる君たちはそれぞれの学習レベルがあります。
わかる人はさらっと確認し、不安な人は読み込んでください。
aIRaの講義は訪れてくれたすべての学ぶ人に“付加価値”を提供します。
早く、多く『周回すること』の楽しさと『効率の高さ』を感じることができますように
……それじゃ、始めましょう!ʕ•̀ᴥ•́ʔو ̑̑
Diels-Alder 反応とは
Diels-Alder反応の重要なポイントまとめ

ここでは、この講義で必ず押さえてほしいポイントを先にまとめておきます。
まだよくわからない人も、この記事を読み終わったあとに
もう一度戻ってくると理解が深まりますよ!
① ジエンは s-cis 配座で反応する
Diels–Alder反応は、共役ジエンが s-cis 配座をとったときにはじめて環化できます。
この“配座条件”がまず最優先。
② Diels–Alder反応は 立体特異的である
ジエノフィルの cis/trans 配置は、そのまま生成物の環上に反映されます。
協奏的機構だから途中でひっくり返らないのです。
③ 置換基によって 位置選択性 が生じる
共役ジエンやジエノフィルに電子求引性基や電子供与性基があると、
電荷の偏りによって“どこで結合しやすいか”が決まります。
④ 電子供与性基/求引性基は 反応性(速度) に影響を与える
電子供与性基のついたジエンは電子が豊富になり反応性が上がります。
電子求引性基のついたジエノフィルはより電子不足になり反応性が上がります。
⑤ endo体が優先して生成する(立体選択性)
電子求引性基を持つジエノフィルでは、endo体が早く生成しやすい傾向があります。
この記事では軌道の話はできるだけ使わず、 “電荷・共鳴・配座” の直観でDiels-Alder反応を理解します。
#U7 で同じ内容をフロンティア軌道論で見直すよ!
まずはDiels-Alder 反応を一言で説明
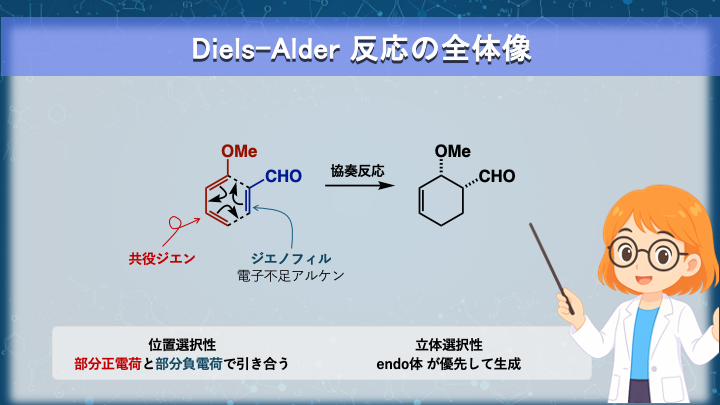
反応の全体像を先に一文で押さえておくと、
この先の理解がとても楽になります。
Diels–Alder反応とは、
“共役ジエンの4電子”と“ジエノフィルの2電子”が
ぐるっと環を一周して、協奏的に
6員環(主にシクロヘキセン)を一挙に構築する反応です。
ジエンの4電子、ジエノフィルの2電子が反応に関わることから、
[4+2]付加環化反応と呼ばれています。
弱い3本のπ結合から、
強いσ結合2本+π結合1本へと変わるため、
エネルギー的にも有利な反応です。弱い3本のπ結合から、
強いσ結合2本+π結合1本へと変わるため、
エネルギー的にも有利な反応です。
協奏反応とは、すべての結合形成・切断が同時に進むタイプの反応です。
詳しくはこちらで解説しています。ぜひ復習してくださいね!
共役ジエンとジエノフィルとは
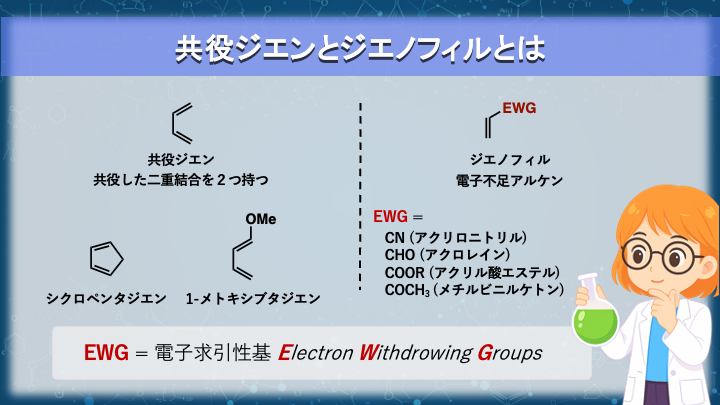
ここからは反応の登場人物を整理します。
共役ジエン(diene)
共役した二重結合を2つ持つ分子のことです。
Diels–Alder反応では必ず s-cis 配座で関与します(後で説明します)。
ジエノフィル(dienophile)
“–phile(〜を好む)”の語源を持ち、
ジエンと反応しやすいアルケン(またはアルキン) を指します。
通常の付加環化であれば
典型的なジエノフィルは、二重結合に
電子求引性基 (CN、CHO、COOR、COR など)
が結合しており、これによって
電子的に“受け取り側”として反応しやすくなります。
図には代表的なジエノフィルを示しました。
(アクリロニトリル、アクロレイン、アクリル酸エステル、
メチルビニルケトン など)
電子不足のアルキンがジエノフィルとして働く場合もあります。
ビニル基がついたカルボン酸誘導体にはアクリルという慣用名がついているね!
① ジエンは s-cis 配座で反応する
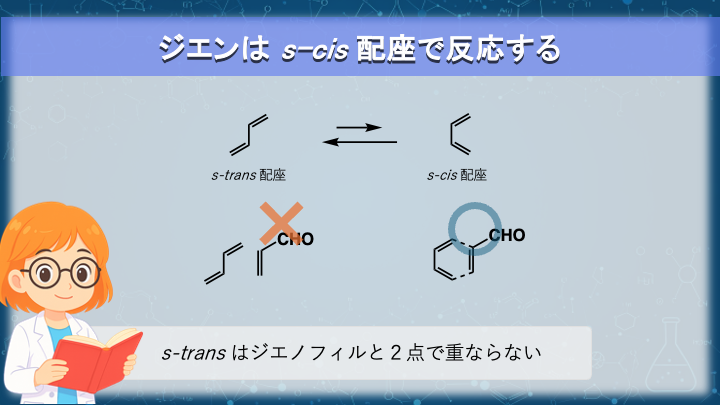
🔹 鎖状ジエンには 2 種類の立体配座がある
共役ジエン(C=C–C=C)は、
中央の単結合が回転できるため 2 種類の配座 をとれます。
- s-cis 配座:
中央の単結合をはさんで、二つの二重結合が「同じ側」 (cis) にある - s-trans 配座:
二つの二重結合が「反対側」 (trans) にある
s-cis の “s” は single bond(単結合)を意味しています。
どちらの配座でも 4 つの炭素はほぼ同一平面上に並び、
共役はどちらでも成立します。
🔹 では何が違う? → s-cis だけが反応に“参加可能”
Diels–Alder反応では、
新しい σ結合を2本、同時に・近い位置で形成する必要があります。
そのためには、
二つの二重結合が 内側に折れ込んだ s-cis 配座になっていなければ
ジエノフィルと結合位置が物理的に届きません。
- s-cis → 反応可能
- s-trans → 物理的に結合形成位置が届かないので反応不能
つまり、ジエンは反応前に
不利な s-cis 配座にいったん変換される必要があるのです。
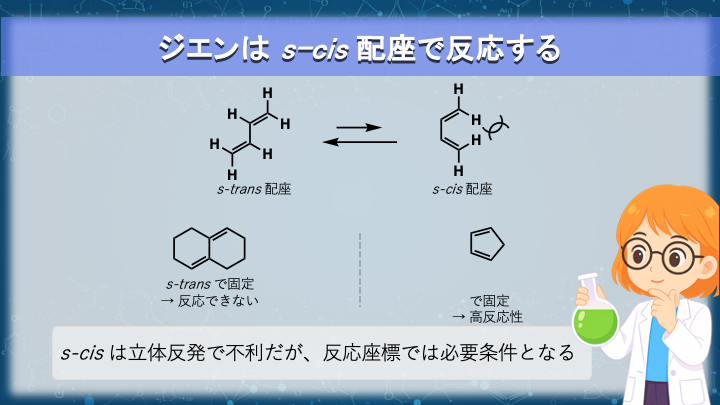
🔹 s-cis は立体的に不利(だから普段は少ない)
s-cis 配座では末端の置換基が接近し、
立体反発が大きくなります。
そのため、鎖状ジエンは
通常 s-trans が優勢です。
反応のためには
「わざわざ不利な姿勢に変わる」
必要があるため、反応性が落ちてしまいます。
🔹 s–cis/s–trans に固定されているジエン
シクロペンタジエンは特に反応性の高いジエンです。
理由はシンプルで、強制的に s-cis 配座に固定されているから。
環状構造のおかげで、
s-cis ⇄ s-trans の平衡が存在せず、
**「常に反応可能な形で待機している」**状態なのです。
一方で、図に示したような 固定 s-trans ジエン は
反応に必要な形に曲がれないため、
Diels–Alder 反応が起こりにくい。
これが
“配座が反応性を決める”
という Diels–Alder の最重要ポイントの一つです。
ジエンの配座は慣れてくると足元すくわれがちな重要なポイント。
Diels-Alderの説明をするときはまずここから!
② Diels–Alder反応は 立体特異的である
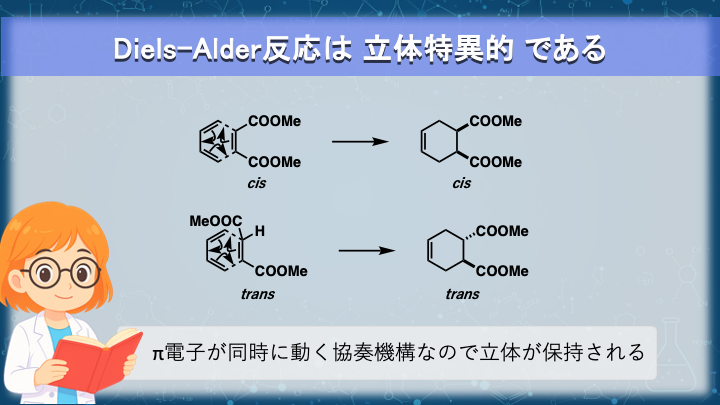
Diels–Alder反応では、
反応前のジエン・ジエノフィルが持っている 置換基の相対配置(cis/trans) が
そのまま生成物の六員環に反映されます。
段階的で回転可能な中間体を経由すると、
立体特異性は発現しないはずですが、
実際にはきれいに対応します。
- ジエノフィルが trans → 生成物も trans
- ジエノフィルが cis → 生成物も cis
この“相対配置の保存”は、
Diels–Alder反応がすでに学んだ 協奏的機構(#U3)の流れに従う反応であることを
明確に示す現象です。
③ 置換基によって 位置選択性 が生まれる
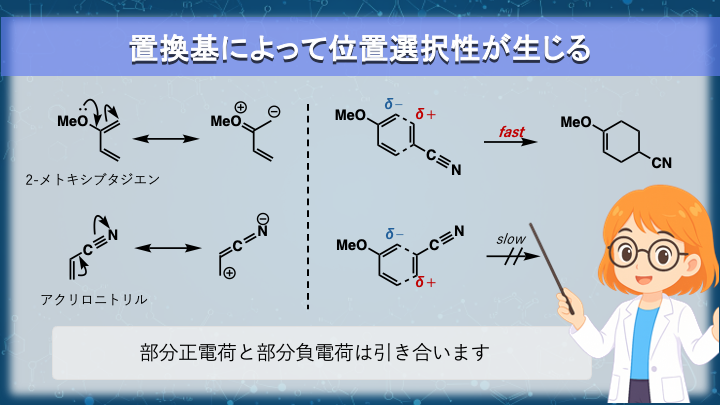
ジエンとジエノフィルが非対称の場合、
結合の仕方は 理論上 2 パターン 存在します。
どちらが主生成物になるかは、
共鳴寄与体から読み取れる電荷分布 で説明できます。
ジエンは4電子あるので電子豊富であり、ジエノフィルは電子を受け取る側であることが前提としてあります。
ジエンとジエノフィルの電子環境を一緒に確認していきましょう
図に示したように、
- アクリロニトリル の β位には部分正電荷
- 2-メトキシ-1,3-ブタジエン の端(1位)には部分負電荷
が生じます。
δ+ と δ− 同士が引き合う組み合わせが優先されるわけですね。
共鳴寄与体を正しく書くことができるかな?動かすのは電子だけ。原子は動いちゃダメだよー
④ 電子供与性基/求引性基は反応性(速度)を左右する
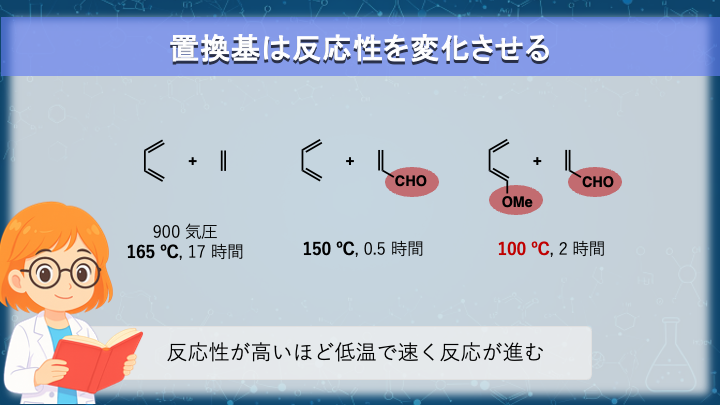
置換基は 生成物の位置選択性だけでなく、反応速度にも直接影響 します。
基本となるのはすでに述べた極性の関係です。
ジエンは電子豊富、ジエノフィルは電子不足。
この電子バランスを置換基がどちら側に傾けるかで反応性が決まります。
- ジエンに電子供与性基
→ ジエンがさらに電子豊富になり、反応性が上がる - ジエノフィルに電子求引性基
→ ジエノフィルがより電子不足になり、反応性が上がる
電子を渡す化学種に電子供与性基を導入すると反応性は向上する。
電子を受け取る化学種に電子求引性基を導入すると反応性は向上する
聞けば当然のことですがいざ質問されると答えられない人も多いです。
ジエンに電子求引性基、ジエノフィルに電子供与性基が導入されると反応性はどうなる?予想してみよう。
⑤ endo体が優先して生成する(立体選択性)
環状ジエンを使うと 架橋二環式化合物 が生成します。
このようなとき、いわゆるendo体/exo体と呼ばれるジアステレオマーを生成します。
どちらがより優先して生成するか?
結論から言うと、endo体が早く生成するので優先して生成します。
このように、一方のジアステレオマーがより多く生成する性質のことを
ジアステレオ選択性と言います
endo体/exo体とは
まずendo/exo とはなんなのか?
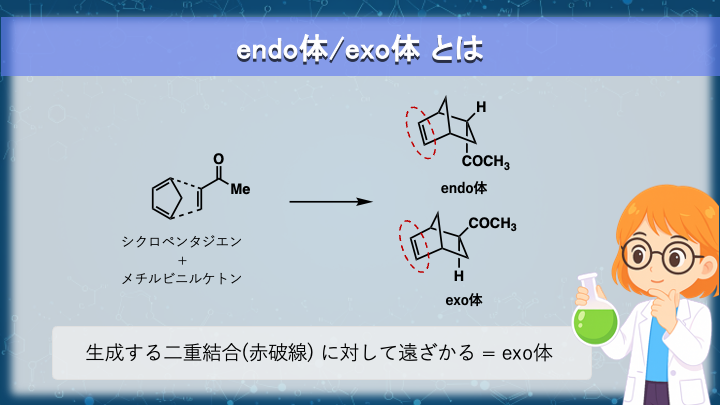
例として、シクロペンタジエンとメチルビニルケトンの反応では、
置換基が “二重結合側を向く構造” と “外側を向く構造” の 2 種類が可能です。
- endo … 置換基が “二重結合側(内側)”
- exo … 置換基が “二重結合から離れる方向(外側)”
ブルースでの定義としては、付加環化反応で生成するπ結合に対して遠ざかる方向に向いているか(exo)、向いていないか(endo)で判別されます。
ただ、この言い回しは初学者には直感的ではないかもしれません。
見分ける、覚えるのが難しい!そんな悩みに文字通りaIRa流の見方を伝授していきます。
endo/exo の aIRa流・見分け方
コツはひとつだけ。
“元のジエン側” から生成物を覗き込む視点に切り替えること。
環状ジエンの「内側, 二重結合側」に置換基が向いていれば endo。
「外側, 二重結合から離れる方向」に向いていれば exo。
語源も合わせると覚えやすくなります。
- endo:内側(endocytosis=取り込む)
- exo:外側(exoskeleton=外骨格、exit=外へ)
自分の見やすい角度で、判別しやすい角度で観察するだけ!
ちょっとだけ、遠回りして余計な知識とリンクさせて、納得できる形で暗記するのがaIRa流です(๑˃̵ᴗ˂̵)
Diels–Alder反応は endo 選択的である
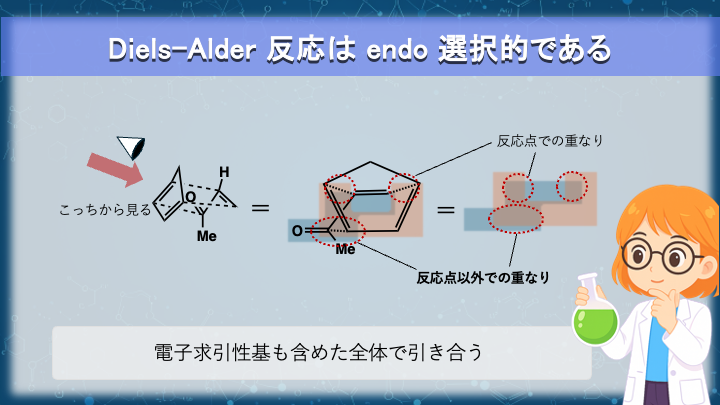
次に、なぜ endo 体が優先するのでしょうか。
理由をひとことで言えば、
遷移状態で“ジエンのC2位”と“ジエノフィルの電子求引性基”が引き合い、
endo 側がより安定するから。
ここでは入門編として、直感的な理解に限定して説明します。
ジエンは 4π電子で電子豊富、
電子求引性基を持つジエノフィルは 電子不足。
反応全体としては “ジエン → ジエノフィル” に電子が流れます。
重要なのは、それぞれが 共役系全体として 電子豊富・電子不足を示すこと。
つまり、
- ジエン(4炭素全体)が δ−
- ジエノフィル+電子求引性基の領域が δ+
となり、σ結合を形成する炭素以外の位置でも
“全体として引き合う配置” が遷移状態を安定化します。(endo則)
今回は入門編です。本当は分子軌道論を含めた解釈が大事になっていますが、 まず初めは感覚的な理解から順番にアップデートさせていきましょう
基礎編を学習した後にもう一度入門編を読んでみると、1周目より理解できるはず。初めはよくわからないのは全員一緒だよ!
まとめ
① ジエンは s-cis 配座で反応する
② Diels–Alder反応は 立体特異的である
③ 置換基によって 位置選択性 が生まれる
④ 電子供与性基/求引性基は 反応性(速度) を左右する
⑤ endo体が優先して生成する(立体選択性)
最後に
今日も有機化学のお勉強、お疲れさま〜( ̄▽ ̄)b☆
反応機構がシンプルに見える分、じつは丁寧に理解しようとすると
意外と手強い範囲なんですよね。
1周目でも10周目でも、読んだ今日にだけ生まれる“気づき”があれば嬉しいです( ˘͈ ᵕ ˘͈ )
入門編を読み切ったあなたへ──
小休憩したら、次は 基礎編 #U7 に進んでみましょう!
基礎編では、この入門編とまったく同じ構成で、
分子軌道論をほんの少しだけ足しつつ、
ワンランク上の視点 で Diels–Alder をもう一度組み立て直します。
同じ流れ、同じ順番で、
別レベルの説明が読める教材はこれまで記事としてありませんでした。
ブルース教テンだけで味わえる、 “効率のよさ” を実現できるはず。
復習しながら、次のレベルにステップアップできる
こんなに効率的な付加環化の学び方、ある?
……ありません! ( •̀ω•́ )✧
さぁ、一緒に Diels–Alder反応を周回していきましょう💫
あなたにとって、有機化学が少しでも笑える世界になりますように。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡















コメントを残す コメントをキャンセル