アルケンの反応③:マルコフニコフ則と転位反応
(ブルース有機化学 第7版/邦訳第5版 p231–250 準拠)
- マルコフニコフ則を“カルボカチオンの安定性”から説明できる
- 超共役と電子の非局在化の違いを整理できる
- 転位反応を「安定化への移動」として直感的に説明できる
有機化学の“楽しみ方”を身につけることを目標に、
一つひとつの反応を丁寧に理解し、異なる視点から解説します。
教科書を10回読んだ博士学生 aIRa が、
ブルース有機化学を軸に「理解でつなぐ大学有機化学」をかわいくお届けします。
🌸 導入

昔から「不死鳥マルコ」というキャラが好きでした。
初登場ではその圧倒的な強さと“再生する不死鳥”という最強設定に驚かされましたが、
若かりし頃のエピソードでは、まだ成長途中の姿も描かれています。
どんな“強キャラ”にも、最強能力よりも大切な「経験の積み重ね」があるのだと感じます。
化学の世界にも、そんな最頻出・最強クラスの“マルコ先生”がいます。
その名も ウラジーミル・マルコフニコフ(Vladimir Markovnikov)。
彼の残した「マルコフニコフ則」は、有機化学反応において反応の位置選択性を説明する重要な理論です。
ですが、多くの学生が「水素は水素の多い方へ付く」と暗記して終わりにしてしまうのも事実。
この法則はもともと経験則から始まりましたが、のちに多くの研究者の再解釈を経て、
現在ではカルボカチオンの安定性という理論的裏付けをもって理解されています。
今回はこの「マルコフニコフ則」を、“暗記”ではなく“理解”で学ぶために、以下の流れで整理します。
- マルコフニコフ則とは
- カルボカチオンの安定性
- カルボカチオン転位反応
- 部分正電荷を持つ反応系での位置選択性
博士課程 aIRa と一緒に学習していきましょう!
🧬 (1) マルコフニコフ則とは
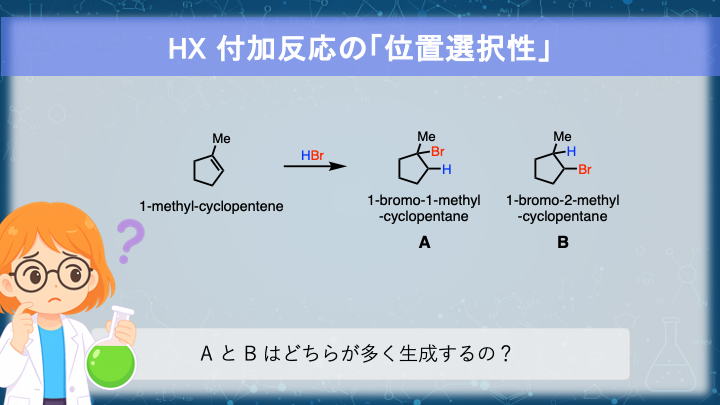
マルコフニコフ則(Markovnikov’s rule)は、非対称アルケンに HX(HCl, HBr, HI など)が付加する際の生成物の方向性を示す経験則です。
ブルースでは次のように定義されています:
「水素原子は、すでにより多くの水素原子が結合している炭素に付加する。」
この経験則はもともとハロゲン化水素(HX)の付加で提唱されましたが、水和反応やハロヒドリン生成など、他の極性付加反応にも同じ考え方が応用されます。
簡単な問題に回答するためだけに暗記するなら、「H は水素の多い炭素に、X は水素の少ない炭素に付く」という経験的法則です。
たとえば、1-メチルシクロペンテンに臭化水素を加えると、次の 2 つの生成物が考えられます。
- A:1-ブロモ-1-メチルシクロペンタン(主生成物)
- B:1-ブロモ-2-メチルシクロペンタン(副生成物)
実際には A が多く生成します。なぜこの選択性が生じるのか。
ここから先が大学有機化学です。
それを理解するには、途中で生成するカルボカチオン中間体の安定性を考える必要があります。
⚡️ (2) HX付加反応とカルボカチオンの安定性
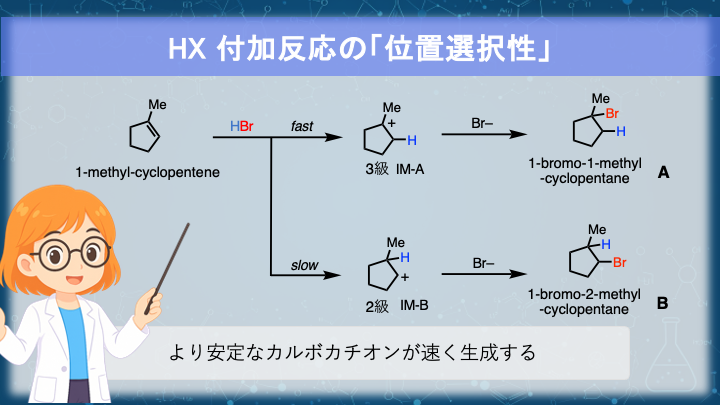
1-メチルシクロペンテンに HBr を付加すると、反応経路によって 2 種類のカルボカチオンが中間体として生じます(IM-A, IM-B)。
- IM-A: 第三級カルボカチオン(正電荷炭素に炭素置換基が 3 つ)
- IM-B: 第二級カルボカチオン(置換基が 2 つ)
IM-A の方が IM-B より安定なので、A 経路の方の生成速度が速く、主生成物となります。
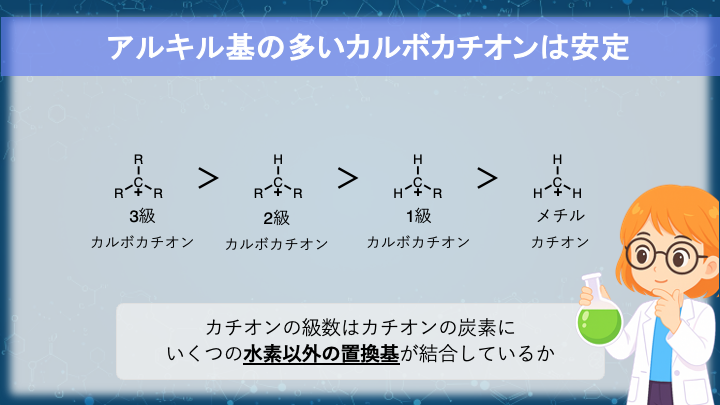
一般に、カルボカチオンの安定性は 第3級 > 第2級 > 第1級 > メチル の順で高いことが知られています。
ここで終わらせてしまう学生が多いですが、実際に理解すべきは次の 2 点です。
- なぜカルボカチオンの安定性に差が出るのか?
- なぜ中間体の安定性が生成物比に影響を与えるのか?
🔄 (3) カルボカチオンの安定性 ― 超共役と電子の非局在化
カルボカチオンの安定性は、主に次の 2 つの要素で説明されます。
- (1) 超共役(hyperconjugation)
- (2) 電子の非局在化(delocalization)
(3-1) 超共役 ― σ結合からの電子分散
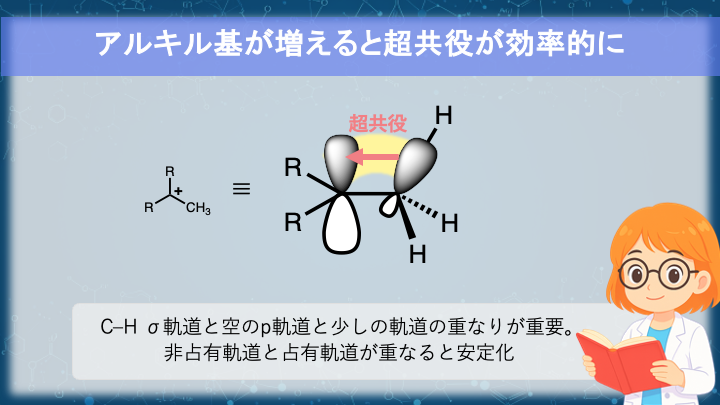
超共役とは、隣接する C–H(または C–C)σ結合の電子が、カルボカチオン中心の空の p 軌道にわずかに分散する現象です。
σ結合軌道の末端が、正電荷を持つ炭素の空p軌道と平行に近い配置を取るとき、電子密度が部分的に共有されます。
つまり、隣にアルキル基が多いほど分散に関与できる σ 結合が増え、より安定になります。
この現象は「弱い電子供与効果」としても説明されます。

縮環で固定されていることで超共役の効果が変化することもあります。
複雑な化合物の場合は模型を組んでみましょう!
(3-2) 電子の非局在化 ― π結合・孤立電子対との共鳴
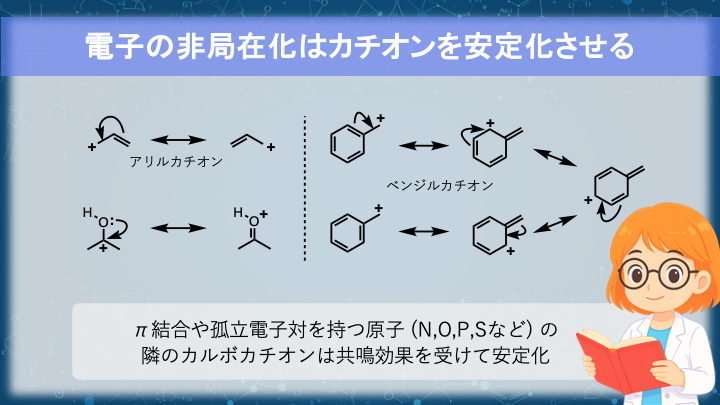
カルボカチオンが π結合 や 孤立電子対を持つ原子(O, N, S など)の隣にある場合、電子が広範囲に分布でき、さらに強い安定化が起こります。
先ほどの超共役と比較してこちらは部分的な軌道の重なりではなく、並行なp軌道同士の重なりで、完全なπ結合を形成します。
電子が非局在化できる厳密な条件は、芳香属性と一緒にブルース第8章を扱うときに丁寧に説明しますね!
- ベンジル位・アリル位・プロパルギル位のカチオン:π系への電荷分散で安定化。
- ヘテロ原子(O, N, S)隣接:孤立電子対の供与(共鳴)で強く安定化。

ベンジル位、アリル位、プロパルギル位は特定の位置を指す用語。
化学言語としてしっかり覚えましょう!
🧩 (4) なぜ中間体の安定性が生成物比に効くのか
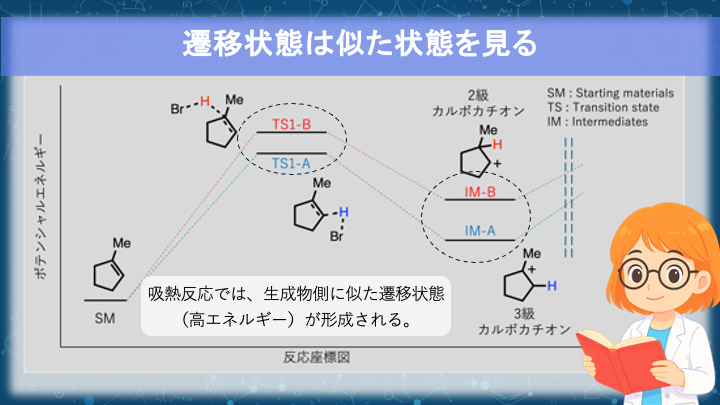
ここが案外軽視されがちな疑問です。中間体の安定性の話が、なぜ生成物比の話に繋がるのか?
この関係は、反応座標図・Hammond の仮説・速度論的支配の 3 つで説明できます。
- HX付加反応の反応座標図を書く。
- 反応速度を決める律速段階は、最初のプロトン付加によるカルボカチオン生成。
- Hammond の仮説:吸熱的な段階では、遷移状態は直後の中間体(カルボカチオン)に似る。
- よって、より安定なカチオンに繋がる経路ほど遷移状態のエネルギーが低く、より速く進行する。
したがって、速度論的支配条件では、安定なカルボカチオンを経る経路の生成物(A)が主生成物となるのです。
ここでは反応の速さ(速度論)が支配的ですが、平衡が成立する条件では生成物の安定性(熱力学的支配)が優先する場合もあります。
速度論的支配、熱力学的支配については#Bで取り扱う予定なので、続報をお待ちください
🔁 (5) 転位反応 ― カルボカチオンは動く
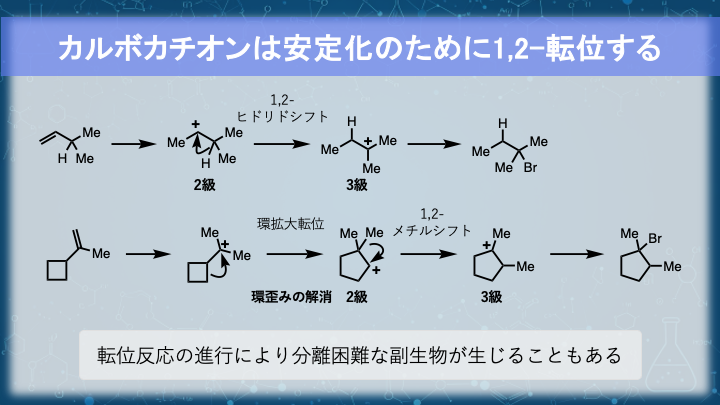
カルボカチオンを経由する反応では、しばしば 1,2-転位 が起こります。
これは、隣接する原子団(H⁻ や CH₃⁻)が電子対ごと移動して、より安定なカチオンに変わる反応です。
主な 2 種類:
- 1,2-ヒドリド転位(H⁻ が移動)
- 1,2-メチル転位(CH₃ 基が移動)
ヒドリド転位では電子対のまま水素が移動するため立体は保持されますが、アルキル転位では結合の組み替え過程で反転を伴うこともあります。
例:3-メチル-1-ブテン + HBr。
初めに第2級カチオンが生成し、1,2-ヒドリド転位で第3級カチオンに変化してブロモイオンに捕捉され、
2-ブロモ-2-メチルブタンが得られます。
また、アルキル転位によって 環拡大や環縮小 が進み、全体として歪みが減少する場合もあります。
一般に、5員環・6員環は安定ですが、3員環・4員環・8員環以上は転位で安定化しやすい傾向にあります。

なぜ 3,4,8 員環が転位しやすいのか「環歪み」というキーワードを使って
説明できますか?
💧 (6) ハロヒドリン形成と部分正電荷の安定性
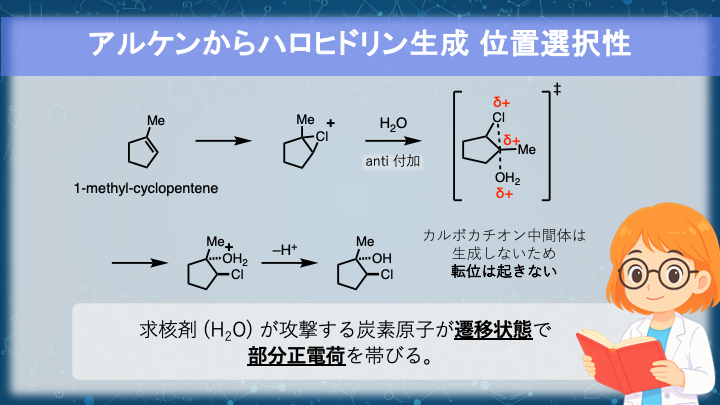
最後に、明確なカルボカチオンを経ない反応でも、同じ安定化の考え方が使えることを確認しましょう。
例:1-メチルシクロペンテンを塩素水溶液と反応させた場合。
まず クロロニウムイオン(三員環中間体) ができ、続いて 水分子が反対側(アンチ付加)から攻撃してクロロヒドリンが生成します。
遷移状態では、塩素から酸素へ正電荷が部分的に移動しています。
この “部分正電荷” も安定化の影響を受けます。
ここでいう“部分正電荷”とは、電子の偏り(分極)によって生じる局所的な電荷のことです。置換基の電子供与性が強いほど、この分極を安定化できます。
したがって、水は より置換の多い炭素を攻撃し、対応する生成物を与えます。
ただし、この反応では明確なカルボカチオンを経ないため、転位は起こりません。

酸性条件のエポキシドへの求核攻撃も同様に説明できますね!
詳しくは11章で説明します!
✏️ まとめ
- マルコフニコフ則はカルボカチオンの安定性を反映した経験則。
- 安定性の差は主に超共役と電子の非局在化で説明される。
- Hammond の仮説により、カチオン安定性の比較は律速段階の遷移状態の比較に等価。
- カルボカチオンは、より安定なカチオンが得られるように転位(1,2-ヒドリド/メチル)する。
- ハロヒドリン形成では部分正電荷の安定化が位置選択を決め、アンチ付加で進行する。
🌸 最後に
今日もお疲れ様でした!今回は、反応の「位置選択性」を決める理論を整理しました。
「この反応も同じ理屈で説明できるかな?」と考えるクセをつけておくと、
どんな反応も理論で理解できるようになります。
次回はあえて、マルコフニコフに“反抗”してみましょう。
私も昔、かーさんと一緒にお父さんに反抗していたので(笑)反抗期重要!!
博士 aIRa と一緒に、化学界のもう一つの法則を見に行きましょう。
それでは、またねーーー〜 (๑˃̵ᴗ˂̵)و♡
日本中の科学の発信がここで確認できます。
みんなでブログを盛り上げましょう!
↓クリック








コメント